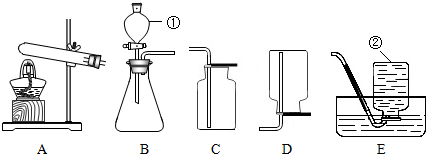
��Ŀ����
ij��ѧʵ��С���ͬѧΪ��̽��ʵ�����о����������ƹ���ijɷ֣��������й�ʵ�飬����������ǽ��е�̽�����
����������衿
�����ȫ����NaOH��
�����ȫ����Na2CO3
����� ��
��ʵ����̽����
��1��ʵ�����£�
��2��Ϊ�˽�һ������֤��������С��ͬѧ���������ʵ�鷽���������������ʵ�飬���ˣ�Ȼ������Һ�еμ���ɫ��̪��Һ������̪��죬���������������̪����죬�����������
С��ͬѧ������С��ͬѧ�ķ�����������ɣ�ͨ����������֪�����Ȼ�����Һ�����ԣ�����ʹ��ɫ��̪��Һ��죬��̼������Һ�� �ԣ���ᡱ��������ʹ��̪��죮��ˣ�����Ϊ�÷����IJ���������Ӧ�øĽ����� ��
����˼�뽻�������ù����������Ʊ��ʵ�ԭ���ǣ��û�ѧ����ʽ��ʾ�� ��
����չ�����졿
��3��ȡ10g�ѱ��ʵ��������ƹ����ڸ�����ձ��У��������м���100gһ������������ϡ���ᣬ��ַ�Ӧ��Ƶ���Һ������Ϊ107.8g��������㣺
��û�з������ʵ��������Ƶ�������
��������Һ�����ʵ�����������
����������衿
�����ȫ����NaOH��
�����ȫ����Na2CO3
�����
��ʵ����̽����
��1��ʵ�����£�
| ʵ��������� | ʵ������ | ���ۼ����� |
| ����һ��ȡ����������Ʒ���Թ��У�������ˮ��ȫ�ܽ⣬Ȼ�����������ϡ���ᣮ | ʵ�������ʼ��û�����ݲ����� | ��֤����������� |
| �������ȡ����������Ʒ���Թ��У�������ˮ��ȫ�ܽ⣬Ȼ��μ�����������Һ�� | ʵ������в��� |
��֤���������������˹����з�����Ӧ�Ļ�ѧ����ʽΪ |
С��ͬѧ������С��ͬѧ�ķ�����������ɣ�ͨ����������֪�����Ȼ�����Һ�����ԣ�����ʹ��ɫ��̪��Һ��죬��̼������Һ��
����˼�뽻�������ù����������Ʊ��ʵ�ԭ���ǣ��û�ѧ����ʽ��ʾ��
����չ�����졿
��3��ȡ10g�ѱ��ʵ��������ƹ����ڸ�����ձ��У��������м���100gһ������������ϡ���ᣬ��ַ�Ӧ��Ƶ���Һ������Ϊ107.8g��������㣺
��û�з������ʵ��������Ƶ�������
��������Һ�����ʵ�����������
���㣺ʵ��̽�����ʵ���ɳɷ��Լ�����,�й��������������ļ���,��Ļ�ѧ����,�εĻ�ѧ����,���ݻ�ѧ��Ӧ����ʽ�ļ���
ר�⣺��ѧ̽��
����������������衿
�������ȫ����NaOH��Ҳ����ȫ����Na2CO3��Ҳ������NaOH��Na2CO3��
��ʵ����̽����
��1��̼���ƺ�ϡ���ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼��
̼���ƺ�����������Ӧ����̼�ᱵ�������������ƣ�
��2��̼������Һ������������Һ���Լ��ԣ����ܹ�ʹ��̪��Һ���ɫ��
�Ȼ�����̼���Ʒ�Ӧ����̼�ᱵ�������Ȼ��ƣ�
���������ܹ����տ����еĶ�����̼�������ܺͶ�����̼��Ӧ����̼���ƺ�ˮ��
��3����Ӧǰ��������Ϊ��Ӧ���ɶ�����̼�����������ݶ�����̼���������Լ���̼���Ƶ��������Ȼ������������һ�����Լ���û�з������ʵ��������Ƶ�������������Һ�����ʵ�����������
�������ȫ����NaOH��Ҳ����ȫ����Na2CO3��Ҳ������NaOH��Na2CO3��
��ʵ����̽����
��1��̼���ƺ�ϡ���ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼��
̼���ƺ�����������Ӧ����̼�ᱵ�������������ƣ�
��2��̼������Һ������������Һ���Լ��ԣ����ܹ�ʹ��̪��Һ���ɫ��
�Ȼ�����̼���Ʒ�Ӧ����̼�ᱵ�������Ȼ��ƣ�
���������ܹ����տ����еĶ�����̼�������ܺͶ�����̼��Ӧ����̼���ƺ�ˮ��
��3����Ӧǰ��������Ϊ��Ӧ���ɶ�����̼�����������ݶ�����̼���������Լ���̼���Ƶ��������Ȼ������������һ�����Լ���û�з������ʵ��������Ƶ�������������Һ�����ʵ�����������
����⣺����������衿
�������ȫ����NaOH��Ҳ����ȫ����Na2CO3��Ҳ������NaOH��Na2CO3��
���NaOH��Na2CO3��
��ʵ����̽����
��1��ȡ����������Ʒ���Թ��У�������ˮ��ȫ�ܽ⣬Ȼ��μ�����������Һ��������ɫ��������֤��������������
̼���ƺ�����������Ӧ�Ļ�ѧ����ʽΪ��Na2CO3+Ba��OH��2�TBaCO3��+2NaOH��
�����ɫ������Na2CO3+Ba��OH��2�TBaCO3��+2NaOH��
��2��̼������Һ�ʼ��ԣ���ʹ��̪��죬��ˣ��÷����IJ���������Ӧ�øĽ����ǣ�ȡ����������Ʒ���Թ��У�������ˮ��ȫ�ܽ⣬Ȼ��μ��������Ȼ�����Һ��
����ȡ����������Ʒ���Թ��У�������ˮ��ȫ�ܽ⣬Ȼ��μ��������Ȼ�����Һ��
����˼�뽻����
�������ƺͶ�����̼��Ӧ�Ļ�ѧ����ʽΪ��2NaOH+CO2�TNa2CO3+H2O��
���2NaOH+CO2�TNa2CO3+H2O��
����չ�����졿
��3������̼���Ƶ�����Ϊx���Ȼ��������Ϊy��
���ɶ�����̼������Ϊ��10g+100g-107.8g=2.2g��
Na2CO3+2HCl�T2NaCl+H2O+CO2����
106 73 44
x y 2.2g
=
=
��
x=5.3g��y=3.65g��
û�з������ʵ��������Ƶ�����Ϊ��10g-5.3g=4.7g��
��û�з������ʵ��������Ƶ�����Ϊ4.7g��
��������Һ�����ʵ���������Ϊ��
��100%=3.65%��
��������Һ�����ʵ���������Ϊ3.65%��
�������ȫ����NaOH��Ҳ����ȫ����Na2CO3��Ҳ������NaOH��Na2CO3��
���NaOH��Na2CO3��
��ʵ����̽����
��1��ȡ����������Ʒ���Թ��У�������ˮ��ȫ�ܽ⣬Ȼ��μ�����������Һ��������ɫ��������֤��������������
̼���ƺ�����������Ӧ�Ļ�ѧ����ʽΪ��Na2CO3+Ba��OH��2�TBaCO3��+2NaOH��
�����ɫ������Na2CO3+Ba��OH��2�TBaCO3��+2NaOH��
��2��̼������Һ�ʼ��ԣ���ʹ��̪��죬��ˣ��÷����IJ���������Ӧ�øĽ����ǣ�ȡ����������Ʒ���Թ��У�������ˮ��ȫ�ܽ⣬Ȼ��μ��������Ȼ�����Һ��
����ȡ����������Ʒ���Թ��У�������ˮ��ȫ�ܽ⣬Ȼ��μ��������Ȼ�����Һ��
����˼�뽻����
�������ƺͶ�����̼��Ӧ�Ļ�ѧ����ʽΪ��2NaOH+CO2�TNa2CO3+H2O��
���2NaOH+CO2�TNa2CO3+H2O��
����չ�����졿
��3������̼���Ƶ�����Ϊx���Ȼ��������Ϊy��
���ɶ�����̼������Ϊ��10g+100g-107.8g=2.2g��
Na2CO3+2HCl�T2NaCl+H2O+CO2����
106 73 44
x y 2.2g
| 106 |
| x |
| 73 |
| y |
| 44 |
| 2.2g |
x=5.3g��y=3.65g��
û�з������ʵ��������Ƶ�����Ϊ��10g-5.3g=4.7g��
��û�з������ʵ��������Ƶ�����Ϊ4.7g��
��������Һ�����ʵ���������Ϊ��
| 3.65g |
| 100g |
��������Һ�����ʵ���������Ϊ3.65%��
�������������ʵ�飬��ѧ�ؽ���ʵ�顢����ʵ�飬�ǵó���ȷʵ����۵�ǰ�ᣬ���Ҫѧ�����ʵ�顢����ʵ�顢����ʵ�飬Ϊѧ�û�ѧ֪ʶ�춨������

��ϰ��ϵ�д�
�����Ŀ
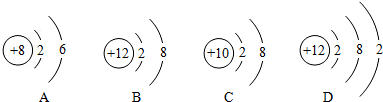
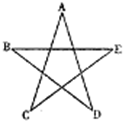 A��B��C��D��E�������ʾ�Ϊ���л�ѧ�г����Ļ��������֮��Ĺ�ϵ��ͼ��ʾ�����߱�ʾ�ܷ�����ѧ��Ӧ��A��C��E��Ϊ�����A�����������һ�����壻ʵ������B����������ȡA����D������������A��C��E��Ӧ������D��
A��B��C��D��E�������ʾ�Ϊ���л�ѧ�г����Ļ��������֮��Ĺ�ϵ��ͼ��ʾ�����߱�ʾ�ܷ�����ѧ��Ӧ��A��C��E��Ϊ�����A�����������һ�����壻ʵ������B����������ȡA����D������������A��C��E��Ӧ������D��