题目内容
【题目】“安全”是生产生活中永恒的主题.如做清洁卫生时,不能将“84消毒液”和洁厕剂混合,否则会产生一种黄绿色的有毒气体--------氯气(Cl2) .
(1)“84消毒液”的有效成分是次氯酸钠(NaClO),其中Cl的化合价为__________;次氯酸钠与盐酸混合后,会生成氯化钠、水及有毒的氯气。写出此反应的化学方程式__________。
(2)目前市场上的洁厕剂大多为酸性,含有一定量的稀酸(如稀盐酸、稀磷酸等),具有腐蚀性,下列物体的表面可用这类洁厕剂清洗的是__________。
A 抽水马桶
B 不锈钢管
C 大理石台面
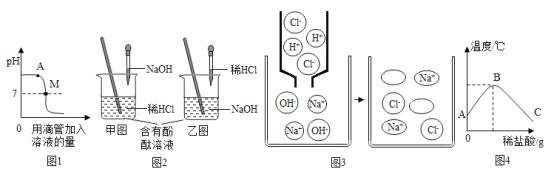
(3)制备“84消毒液”的主要反应为:![]() 。若要证明“84消毒液”中是否含有NaCl,其方法是:取少量“84消毒液”,加入少量____________溶液(填名称),观察是否产生不溶于稀硝酸的白色沉淀。
。若要证明“84消毒液”中是否含有NaCl,其方法是:取少量“84消毒液”,加入少量____________溶液(填名称),观察是否产生不溶于稀硝酸的白色沉淀。
【答案】+1 ![]() A 硝酸银
A 硝酸银
【解析】
(1)次氯酸钠的化学式为NaClO,其中钠元素的化合价为+1价,氧元素的化合价为-2价,根据化合物中正负化合价代数和为0,则Cl的化合价为+1价;次氯酸钠与盐酸混合后,会生成氯化钠、水及有毒的氯气,此反应的化学方程式为![]() 。
。
(2)A、抽水马桶一般是用塑料或陶瓷做的,与酸不反应,且耐腐蚀,符合题意;
B、不锈钢管主要成分是铁,与稀酸会反应,加速钢铁的腐蚀,不符合题意;
C、大理石台面的主要成分是碳酸钙,与稀酸会反应,生成可溶的盐,使大理石台面变得粗糙不平,不符合题意。故选A。
(3)证明“84消毒液”中是否含有NaCl,其实就是证明“84消毒液”中是否含有氯离子,方法是:取少量“84消毒液”,加入少量硝酸银溶液,观察是否产生不溶于稀硝酸的白色沉淀,如果有不溶于稀硝酸的白色沉淀产生,则含有氯化钠,反之则无。

练习册系列答案
相关题目