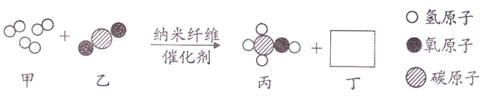
题目内容
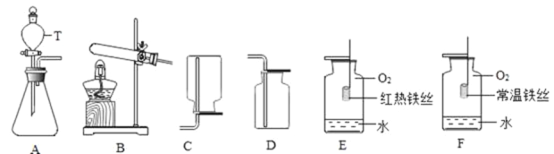
【题目】根据下列装置,回答问题:
(1)写出图中标号仪器的名称:①___________;②___________
(2)实验室用大理石或石灰石和稀盐酸制取二氧化碳时,发生反应的化学方程式为________,从控制反应速率和节约药品的角度考虑,发生装置最好选用_________(填装置序号,下同)
(3)若收集的是氧气,因为氧气不易溶于水,所以可以利用装置________(填装置序号)收集,如果在集气瓶中做铁丝燃烧实验时,发现集气瓶底部炸裂,可能原因是_______,写出铁在氧气中燃烧的化学方程式_________.
【答案】分液漏斗 试管 CaCO3+2HCl=CaCl2+H2O+CO2↑ B F 集气瓶底没有铺细沙或集气瓶中没有放水或燃烧时高温生成物掉落炸裂集气瓶 3Fe+2O2![]() Fe3O4
Fe3O4
【解析】
(1)标号①仪器的名称是分液漏斗,标号②仪器的名称是试管;
(2)实验室用大理石或石灰石和稀盐酸生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,分液漏斗可以控制液体的滴加速度,所以从控制反应速率和节约药品的角度考虑,发生装置最好选用B;
(3)氧气不易溶于水,可以用排水法收集,利用装置F收集,玻璃是热的不良导体,受热不均,会发生炸裂,所以发现集气瓶底部炸裂,可能原因是:集气瓶底部没有放少量的水或细沙,铁和氧气在点燃的条件下生成四氧化三铁,化学方程式为:3Fe+2O2![]() Fe3O4。
Fe3O4。

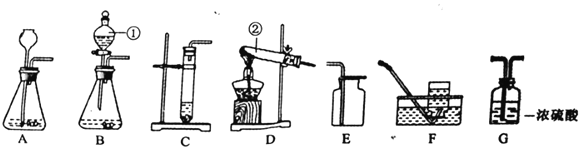
【题目】在学习“分子和原子”时,教师演示了右图所示实验:
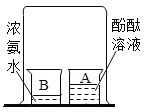
①向烧杯A中加入20mL蒸馏水,再滴入5~6滴酚酞溶液,搅拌均匀,观察到溶液是无色的。
②向烧杯B中加入10mL浓氨水。
③用一个大烧杯罩住A、B两个小烧杯,几分钟后观察到A烧杯中的溶液变红。
[提出问题]A烧杯中的溶液为什么变红?
[进行假设]假设1:浓氨水中的微粒从B烧杯中运动到A烧杯中,使其变红。假设2:_____________________________。
[设计实验]请设计一个实验方案来验证“假设1”是成立的。
假设 | 实验操作 | 实验现象 | 结论 |
假设1 | _____ | _____ | 假设1成立 |
[得出结论]通过以上实验探究,说明了 ___________________________________________________。
[交流与讨论]能说明以上实验结论的实例还有_________________________________举一例即可)。
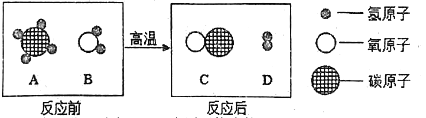
【题目】实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气,写出反应的化学方程式:________________。
小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
(提出猜想)除MnO2、CuO外,Fe2O3也可以作KClO3分解的催化剂。(完成实验)按下表进行实验,并测定分解温度(分解温度越低,催化效果越好)。
实验标号 | 实验药品 | 分解温度(℃) |
① | KCI03 | 580 |
② | KCIO3、MnO2(质量比1:1) | 350 |
③ | KClO3、CuO(质量比1:1) | 370 |
④ | KClO3、Fe203(质量比1:1) | 390 |
(分析数据、得出结论)
(1)由实验________与实验④对比,证明猜想合理;
(2)实验所用的三种金属氧化物,催化效果最好的是________。
(反思)
(1)若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后的质量和__________不变;
(2)同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证。
[提出猜想]质量相同的催化剂,颗粒越细,催化效果越好。
[设计实验]___________________________________________
[结论与反思]颗粒越细,与反应物接触面积越大,催化效果越好。