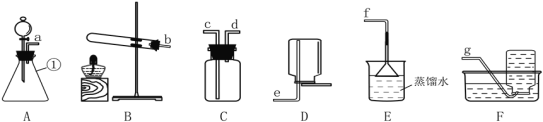题目内容
【题目】某兴趣小组同学对CO和CO2两种常见气体进行如图探究活动。

探究I.实验室制取CO2时,大理石的形状对反应速率的影响。
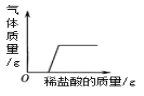
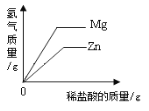
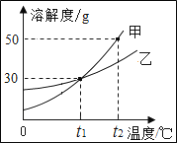
实验1:取等纯度、等质量的块状和粉末状大理石,分别加入足量等浓度的稀盐酸,实验过程中生成气体的体积随时间变化的情况如图1所示。
(1)分析图中_____(选填序号)点,可得出“块状大理石与稀盐酸的反应速率较慢”的结论。
A ac B ab C be D bd
(2)e点表达的含义是_____。
探究Ⅱ,验证CO和CO2的化学性质
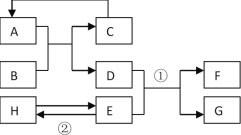
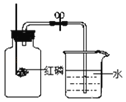
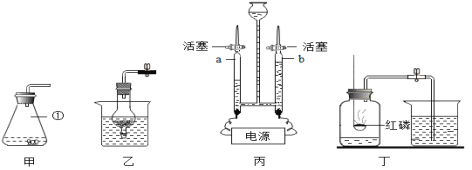
实验2:小组同学按照图2所示装置进行实验,实验前,K1、K2均关闭;实验开始后,打开K2,当装置C中溶液变浑浊时,立即关闭K2,打开K1,观察到装置B中溶液始终无明显变化。
(1)实验过程中观察到装置A中_____,证明CO有还原性。
(2)“装置C中溶液变浑浊”的原因是_____(用化学方程式表示);取少量反应后装置B中的溶液于试管中,加入足量稀盐酸,观察到_____。据此,小组同学得出“CO2能与碱溶液反应”的结论。
(3)装置B、C都能有效防止一氧化碳污染空气,其中装置B中可观察到气球涨大,装置C中与之相关的现象是_____。
探究Ⅲ.探究装置B中反应物是否有剩余
实验3:小红取实验2结束后装置B中的溶液少许,先向其中加入足量的BaCl2溶液,然后滴入酚酞溶液,根据观察到的现象得出“装置B中的氢氧化钠有剩余”的结论。
加入足量BaCl2溶液的作用是_____。
【答案】B 两种形状的大理石和稀盐酸完全反应 黑色固体变红色 Ca(OH)2+CO2═CaCO3↓+H2O 产生气泡 液体压入长颈漏斗 除去碳酸钠,防止影响对氢氧化钠的检验
【解析】
大理石主要成分是碳酸钙,和盐酸反应生成氯化钙、水和二氧化碳;二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,和氢氧化钠反应生成碳酸钠和水;碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,和氯化钡反应生成碳酸钡沉淀和氯化钠;碳酸钠和氢氧化钠的水溶液都是显碱性溶液,都能使酚酞试液变红色。
实验1:(1)分析图中ab点,可得出“块状大理石与稀盐酸的反应速率较慢”的结论,这是因为ab点时,反应时间相等,生成气体越多,反应速率越快。故填B
(2)e点表达的含义是两种形状的大理石和稀盐酸完全反应。故填:两种形状的大理石和稀盐酸完全反应
实验2:(1)实验过程中观察到装置A中黑色固体变红色,证明CO有还原性。故填:黑色固体变红色
(2)“装置C中溶液变浑浊”的原因是二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式:Ca(OH)2+CO2═CaCO3↓+H2O;取少量反应后装置B中的溶液于试管中,加入足量稀盐酸,观察到产生气泡,是因为碳酸钠和盐酸反应生成了二氧化碳,据此,小组同学得出“CO2能与碱溶液反应”的结论。故填:Ca(OH)2+CO2═CaCO3↓+H2O;产生气泡
(3)装置B、C都能有效防止一氧化碳污染空气,其中装置B中可观察到气球涨大,装置C中与之相关的现象是液体压入长颈漏斗。故填:液体压入长颈漏斗
实验3:加入足量BaCl2溶液的作用是除去碳酸钠,防止影响对氢氧化钠的检验。故填:除去碳酸钠,防止影响对氢氧化钠的检验