题目内容
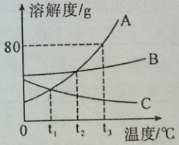
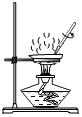
【题目】已知A—H均为初中化学常见的物质。其中A、C是组成元素相同的气体,且C会产生温室效应;B为红棕色固体,D是生产生活中使用最广的金属;F是紫红色金属;H既是一种蓝色沉淀,又是一种碱。 根据如图所示的转化关系(图中反应条件均已略去),请回答:
(1)写出下列物质的化学式:A________、H_______;
(2)写出下列反应的化学方程式:
① ______________________________________;
② ______________________________________,反应②的基本反应类型是_________________。
【答案】CO Cu(OH)2 Fe + CuSO4 == FeSO4 + Cu 2NaOH + CuSO4 == Cu(OH)2 ↓+ Na2SO4 复分解反应
【解析】
A、C是组成元素相同的气体,且C会产生温室效应,因此A是一氧化碳,C是二氧化碳;B为红棕色固体,D是生产生活中使用最广的金属,一氧化碳和红棕色的氧化铁反应生成铁和二氧化碳,因此B是氧化铁,D是铁;F是紫红色金属,因此F是铜;铁和硫酸铜反应生成铜和硫酸亚铁,因此E是硫酸铜,G是硫酸亚铁;H既是一种蓝色沉淀,又是一种碱,因此H是氢氧化铜。
(1)A、C是组成元素相同的气体,且C会产生温室效应,因此A是一氧化碳,C是二氧化碳;H既是一种蓝色沉淀,又是一种碱,因此H是氢氧化铜;故答案为:CO;Cu(OH)2;
(2)①铁和硫酸铜反应生成铜和硫酸亚铁;②氢氧化钠和硫酸铜反应生成氢氧化铜蓝色沉淀和硫酸钠,配平即可,属于复分解反应;故答案为:①Fe+CuSO4=FeSO4+Cu;②2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;复分解反应;(合理即可)

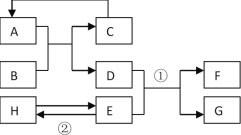
【题目】根据下列实验装置图,回答问题。
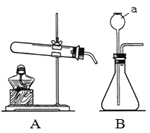
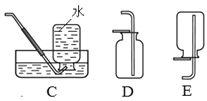
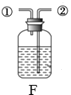
发生装置 | 收集装置 | 洗气装置 |
|
|
|
(1)写出图中仪器a的名称_____。
(2)写出实验室制取CO2的化学方程式_____,发生装置选择_____(填字母),如果要收集干燥的CO2,需要连接F装置,则F装置内加入的试剂是_____(选填“浓硫酸”或“氢氧化钠”),气体从_____(填①或②)端进入。
(3)实验室需少量甲烷,可用加热无水醋酸钠与碱石灰的固体混合物制得。制甲烷的发生装置应选用_____(填字母)装置,收集甲烷可选用C或E装置,由此推断甲烷具有的物理性质是_____。
(4)①实验室用锌与稀硫酸制取氢气并验证其可燃性,实验过程是:组装仪器→检查装置气密性→装入药品制备氢气→_____→点燃。
②氢气的生产方法是制约其作为清洁能源广泛使用的原因之一,科学家根据生产方法提出“绿色”氢气和“有污染”的氢气的概念,下列方法可获得“绿色”氢气的是_____。
A用矿石生产锌和硫酸,再相互反应 B利用风能、水力发电,再电解水
C利用煤燃烧发电,再电解水 D在催化剂作用下,利用太阳能光解水