题目内容
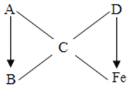
【题目】铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关。
(1)铝、铁、铜中,最早被人们大规模使用的金属是___________。
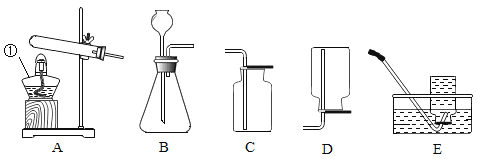
(2)某同学为验证三种金属的活动性顺序设计了如下实验。

①实验前,先用砂纸打磨铝片,其原因是______________(用方程式解释)。
②为达到实验目的,实验a中试剂X应为______________。
A.5mL 5%稀盐酸 B.10mL 5%稀盐酸 C.5mL 5%稀硫酸
③某同学提出也可选用上述金属和一种盐溶液来证明三种金属活动性顺序,则该盐溶液为__________(填名称)。
【答案】 铜 4Al +3O2 = 2Al2O3 A 硫酸亚铁
【解析】本题考查了金属活动性探究。解题时注意控制变量原理的运用。
(1)活动性弱的金属不易发生化学反应,能以单质形式存在,且比较容易冶炼,人类使用金属的顺序与金属的活动性相反,铝、铁、铜中,铝最活泼,铜最不活泼,最早被人们大规模使用的金属是铜;
(2)①铝在空气中易与空气中的氧气反应生成氧化铝,实验前,先用砂纸打磨铝片,其原因是4Al +3O2 = 2Al2O3;
②在相同的条件下,可根据金属与酸反应的剧烈程度来判定金属的活动性。为达到实验目的,实验a中试剂X应为与b、c中相同的5mL 5%稀盐酸。故选A;
③铝能与硫酸亚铁反应,说明铝的活动性大于铁,铜不能与硫酸亚铁反应,说明铁的活动性大于铜。选用上述金属和一种盐溶液来证明三种金属活动性顺序,则该盐溶液为硫酸亚铁。

练习册系列答案
相关题目