题目内容
【题目】在研究某石灰石样品(杂质不溶于水也不与盐酸反应)的活动中,兴趣小组同学进行了如下实验,过程如图所示:
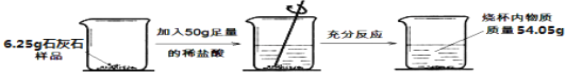
求:(1)反应中生成二氧化碳的质量是_______。
(2)该大理石样品中碳酸钙的质量分数是_______。
(3)100kg这种石灰石充分煅烧后,可得到固体多少kg?(碳酸钙高温分解时只生成氧化钙与二氧化碳)(规范地书写计算过程)_______
【答案】2.2g 80% 64.8Kg
【解析】
(1)根据质量守恒定律,反应中生成二氧化碳的质量是6.25g+50g-54.05g=2.2g。
(2)设该大理石样品中碳酸钙的质量是x,则
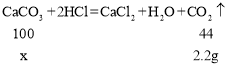
![]() ;
;
答:该大理石样品中碳酸钙的质量分数是![]() 。
。
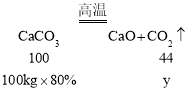
(3)高温煅烧石灰石,其中碳酸钙高温分解时只生成氧化钙与二氧化碳,杂质不参加反应,故样品质量减去生成二氧化碳的质量为得到固体的质量,设生成二氧化碳的质量为y,则
![]()
故100kg这种石灰石充分煅烧后,可得到固体的质量为100kg-35.2kg=64.8kg;
答:100kg这种石灰石充分煅烧后,可得到固体64.8kg。

练习册系列答案
相关题目
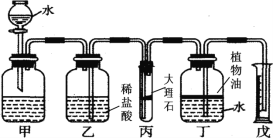
【题目】对下列实指定容器中的水,其解释没有体现水的主要作用的是( )
实验装置 |
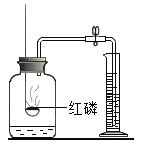
硫在空气中燃烧 |
测定空气中氧气的含量 |
铁丝在氧气中燃烧 |
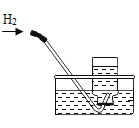
排水法收集氢气 |
解释 | 集气瓶中的水:吸收放出的热量 | 量筒中的水:通过水的体积变化得出氧气的体积 | 集气瓶中的水:冷却溅落熔融物,防止集气瓶炸裂 | 集气瓶中的水:水先将集气瓶中的空气排净,后便于观察H2何时收集满 |
A.AB.BC.CD.D