题目内容
【题目】某纯碱厂生产的某批次碳酸钠产品中可能含有氯化钠杂质。
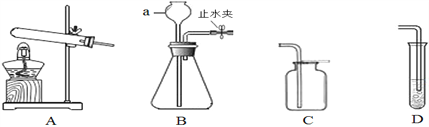
(1)要确定该产品中是否含有杂质氯化钠,你的方法是________。
(2)取该碳酸钠样品12.5 g,将其放入干净的烧杯中,加入100 g水,使其完全溶解。向所得溶液中加入溶 质质量分数为7.3%的稀盐酸,烧杯中溶液的质量与加入稀盐酸的质量关系曲线如图所示。请回答下列问题。
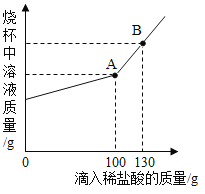
B点时,烧杯中溶液里存在的溶质为_______。
(3)求该碳酸钠样品中碳酸钠的质量分数___。
【答案】(1)取样品于试管中,加入足量的稀硝酸,再加入硝酸银溶液,观察是否产生白色沉淀
(2)HCl和NaCl
(3)84.8%
【解析】
(1)要检验碳酸钠中是否含有氯化钠就需要先排除碳酸钠的干扰,取样品于试管中,加入足量的稀硝酸,再加入硝酸银溶液,观察是否产生白色沉淀;
(2)碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,溶液质量增加,碳酸钠反应完后,不再生成二氧化碳气体,继续加入稀盐酸,增加的质量全部是加入的稀盐酸的质量,溶液质量增大的幅度增大,B点时盐酸过量,所以含有的溶质为氯化氢和生成的氯化钠。故填:HCl和NaCl。
(3)碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,溶液质量增加,碳酸钠反应完后,不再生成二氧化碳气体,继续加入稀盐酸,溶液质量增大的幅度增大。所以A点即为盐酸与碳酸钠恰好反应的时刻,此时消耗盐酸质量为100g,消耗盐酸溶质HCl的质量为100g×7.3%=7.3g,设参加反应的碳酸钠的质量为x,
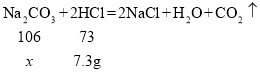
![]() 解得x=10.6g;
解得x=10.6g;
碳酸钠样品中碳酸钠的质量分数=![]() 。
。
答:该碳酸钠样品中碳酸钠的质量分数为84.8%。

练习册系列答案
相关题目