题目内容
某无色溶液中的溶质可能含有Na2SO4、KCl、Mg(NO3)2三种物质中的一种或多种,用它进行以下实验(假设每步均恰好完全反应).
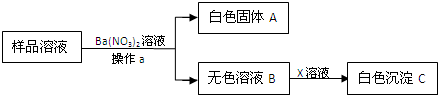
(1)操作a的名称是______.
(2)写出加Ba(NO3)2溶液所发生反应的方程式:______.
(3)如x是AgNO3时,据上图推断,原样品中一定有______.
(4)当x是NaOH时,白色沉淀C是______.
解:(1)通过操作a将白色固体A和无色溶液B分离,根据过滤的原理说明是用过滤的方法加以分离;
故答案为:过滤
(2)能与硝酸钡溶液反应生成沉淀的只有硫酸钠,所以加入硫酸钠溶液发生的反应是硫酸钠和硝酸钡反应生成硝酸钠和硫酸钡沉淀;
故答案为:Na2SO4+Ba(NO3)2=2NaNO3+BaSO4↓;
(3)样品加入硝酸钡溶液可生成白色沉淀,说明一定含有硫酸钠;反应后的溶液B中一定含有硝酸钠,滴加硝酸银溶液可生成白色沉淀,说明B中还含有氯离子,一定有氯化钾;
故答案为:Na2SO4、KCl;
(4)溶液B中一定含有硝酸钠,KCl、Mg(NO3)2两种物质中能与氢氧化钠反应生成沉淀的是硝酸镁,生成沉淀为氢氧化镁;
故答案为:Mg(OH)2
分析:(1)过滤是除去不溶性固体的一种方法;
(2)根据硝酸钡可与硫酸钠反应生成硝酸钠和硫酸钡沉淀书写方程式;
(3)样品加入硝酸钡溶液可生成白色沉淀,说明一定含有硫酸钠;反应后的溶液B中一定含有硝酸钠,滴加硝酸银溶液可生成白色沉淀,说明B中还含有氯离子,一定有氯化钾;
(4)NaOH可与硝酸镁反应生成白色沉淀氢氧化镁,与氯化钾和硝酸钠不反应.
点评:此题主要考查学生对盐的化学性质的掌握和应用能力,不但要求学生具备有关盐的基础知识,而且要有实验操作的经历和分析、解决化学实验问题的能力.
故答案为:过滤
(2)能与硝酸钡溶液反应生成沉淀的只有硫酸钠,所以加入硫酸钠溶液发生的反应是硫酸钠和硝酸钡反应生成硝酸钠和硫酸钡沉淀;
故答案为:Na2SO4+Ba(NO3)2=2NaNO3+BaSO4↓;
(3)样品加入硝酸钡溶液可生成白色沉淀,说明一定含有硫酸钠;反应后的溶液B中一定含有硝酸钠,滴加硝酸银溶液可生成白色沉淀,说明B中还含有氯离子,一定有氯化钾;
故答案为:Na2SO4、KCl;
(4)溶液B中一定含有硝酸钠,KCl、Mg(NO3)2两种物质中能与氢氧化钠反应生成沉淀的是硝酸镁,生成沉淀为氢氧化镁;
故答案为:Mg(OH)2
分析:(1)过滤是除去不溶性固体的一种方法;
(2)根据硝酸钡可与硫酸钠反应生成硝酸钠和硫酸钡沉淀书写方程式;
(3)样品加入硝酸钡溶液可生成白色沉淀,说明一定含有硫酸钠;反应后的溶液B中一定含有硝酸钠,滴加硝酸银溶液可生成白色沉淀,说明B中还含有氯离子,一定有氯化钾;
(4)NaOH可与硝酸镁反应生成白色沉淀氢氧化镁,与氯化钾和硝酸钠不反应.
点评:此题主要考查学生对盐的化学性质的掌握和应用能力,不但要求学生具备有关盐的基础知识,而且要有实验操作的经历和分析、解决化学实验问题的能力.

练习册系列答案
相关题目
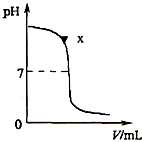 19、某兴趣小组同学对NaOH溶液与稀盐酸发生中和反应进行探究,设计了如下实验:同学们把两种无色溶液分别贴上A、B标签,向烧杯中倒入一定量的A溶液并测定其pH,再向溶液中逐滴加入B溶液,并不断振荡,同时测定混合液的pH,pH变化情况如图.
19、某兴趣小组同学对NaOH溶液与稀盐酸发生中和反应进行探究,设计了如下实验:同学们把两种无色溶液分别贴上A、B标签,向烧杯中倒入一定量的A溶液并测定其pH,再向溶液中逐滴加入B溶液,并不断振荡,同时测定混合液的pH,pH变化情况如图.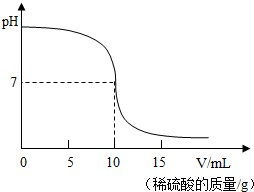 (2013?张家港市模拟)利用中和反应可以测定酸或碱溶液中溶质的质量分数.下图为某次测定过程中,溶液的pH随所滴加的某标准溶液体积的变化而变化的关系图.
(2013?张家港市模拟)利用中和反应可以测定酸或碱溶液中溶质的质量分数.下图为某次测定过程中,溶液的pH随所滴加的某标准溶液体积的变化而变化的关系图.

