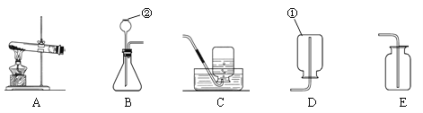
题目内容
【题目】波尔多液泛应用于蔬菜、果树等的病害防治,是由硫酸铜溶液和石灰乳按一定比例混合而成的一种保护性杀菌剂。请回答:

(1)配制波尔多液时,发生反应的化学方程式是______,配制过程中不能用铁制容器,原因是______(用化学方程式表示);
(2)喷洒波尔多液后,不到采摘期的蔬果表面有一些蓝色斑点(一种难溶性喊),蓝色斑点的成分是______(填化学式),不易用水清洗,可用厨房中的调味剂______浸泡除去。
【答案】Ca(OH)2+CuSO4=Cu(OH)2↓+CaSO4 Fe+CuSO4=FeSO4+Cu Cu(OH)2 食醋
【解析】
(1)氢氧化钙能与硫酸铜反应生成氢氧化铜沉淀和硫酸钙,发生反应的化学方程式是:Ca(OH)2+CuSO4═Cu(OH)2↓+CaSO4;
铁能与硫酸铜反应生成硫酸亚铁和铜,发生反应的化学方程式是:Fe+CuSO4=FeSO4+Cu。
(2)波尔多液中两种物质氢氧化钙与硫酸铜相互反应,生成蓝色的氢氧化铜沉淀,不溶于水,形成蓝色斑点,厨房用品中的食醋显酸性,可以和氢氧化铜发生中和反应,将氢氧化铜除去。

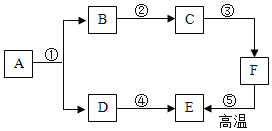
【题目】某研究小组对自动充气气球(如下图1所示)进行下列探究。
(查阅资料)该气球充气原理是通过挤破气球内液体包使液体与白色粉末接触产生二氧化碳气体,实现气球自动充气。

(1)为检验气体是二氧化碳,可选用________(填试剂名称)。
探究一:液体包内溶液酸碱性的探究
(2)室温时,用pH试纸测得溶液pH=3,则该溶液呈酸性。
探究二:白色粉末成分的探究
(猜想与假设)甲同学认为是碳酸钙;乙同学认为是碳酸钠;丙同学认为是碳酸氢钠
(设计并进行实验)
(3)将少量白色粉末放入水中搅拌,固体全部溶解,说明甲同学的猜想_______(填“正确”或“不正确”))。
(4)室温时,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的10%的盐酸(装置如上图2所示),记录如下表。
实验编号 | 锥形瓶内物质 | 最终得到CO2的体积/mL | |
物质 | 质量/g | ||
① | 碳酸氢钠 | 0.10 | V1 |
② | 碳酸钠 | 0.10 | V2 |
③ | 白色粉末 | X | V1 |
实验②的化学方程式为___________;表中X =______g;V1________(填“>”“<”或“=”) V2
(5)分析上表实验数据得出的结论及判断依据是_________。
【题目】在做“铁在氧气里燃烧”实验时,小红等同学进行了以下探究活动,请你一同参与。
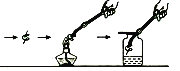
(1)实验时要用砂纸擦去铁丝表面的铁锈,这个过程属于________变化。
(2)小明同学实验时,瓶底放了少量水,但集气瓶仍炸裂了,请你帮助他分析一下可能的原因________。
(3)探究直径为0.38mm的铁丝燃烧是否需要纯氧
(实验内容)取0.38mm的铁丝,分别在体积分数为90%、70%、65%、60%、55%的氧气中进行实验,实验现象如下表所示:
O2的体积分数 | 90% | 70% | 65% | 60% | 55% |
实验现象 | 燃烧剧烈、燃烧时间长,效果好 | 燃烧比90%弱,燃烧时间短,实验成功 | 燃烧比70%弱,燃烧时间比70%短,实验成功 | 燃烧比65%弱,燃烧时间更短,实验成功 | 难以燃烧,只是发红 |
(实验结论):就0.38mm铁丝而言,燃烧所需氧气的最低体积分数为60%,且氧气浓度越大,燃烧现象越________。(填“剧烈”或“不剧烈”);
(实验拓展):(4)上述关于铁丝燃烧所需氧气最低浓度的结论是否合理,请说出理由?
________(填 “合理”或 “不合理”),理由:________。
(5)小红对小明的实验进行了改进,并对铁丝在氧气中燃烧时“火星四射”的现象与其含碳量的关系进行了如下探究。
实验操作 | 实验现象 | 解释与结论 |
实验①:取直径0.20mm,含碳0.1%的铁丝,在氧气中燃烧 | 零星的 火星 | ①写出铁燃烧的文字或符号表达式:____; ②铁丝在氧气中燃烧,“火星四射”与其含碳量的关系为________。 |
实验②:取直径0.20mm,含碳0.32%的铁丝,在氧气中燃烧 | 较明显的 火星四射 |