题目内容
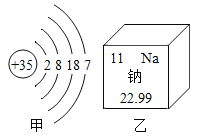
【题目】如图所示,甲是溴(Br)的原子结构示意图,乙摘自元素周期表。说法不正确的是( )
A.甲元素属于非金属元素
B.甲、乙两种元素形成化合物的化学式是NaBr
C.乙元素位于元素周期表中第二周期
D.甲原子在化学反应中容易得到电子
【答案】C
【解析】
A、甲是溴,溴原子最外层电子数是7,元素名称带“氵”旁,属于非金属元素,选项A正确;
B、溴原子的最外层电子数为7,在化学反应中易得到1个电子而形成带1个单位负电荷的阴离子,化合价的数值等于离子所带电荷的数值,则该元素的化合价为-1价;钠元素显+1价,形成化合物的化学式为NaBr,选项B正确;
C、乙元素是钠元素,钠原子核内有11个质子,核外有3个电子层,第一层上有2个电子、第二层上有8个电子,最外层上有1个电子,周期数=原子核外电子层数,所以在元素周期表中,钠元素位于第3周期,选项C不正确;
D、甲原子的最外层电子数是7,在化学反应中易得到1个电子而形成阴离子,选项D正确。故选C。

练习册系列答案
相关题目
【题目】依据下列实验室制取气体的发生和收集装置,选择“I”或“II”进行作答,二者均作答,按“I”进行计分。
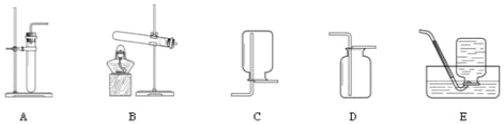
I | II |
(1)实验室用高锰酸钾制取氧气的化学方程式是_____,发生装置选择_____。 (2)氧气可选用E进行收集,其原因是_____。 | (1)实验室制取二氧化碳的化学方程式是_____,收集装置选择_____。 (2)二氧化碳的验满方法是_____。 |