题目内容
 如图为镁条在空气中燃烧时,由镁原子变成镁离子的卡通图.
如图为镁条在空气中燃烧时,由镁原子变成镁离子的卡通图.
请你分析,然后写出从图中获取的两点信息:
①________②________.
化学反应中镁原子易失掉最外层的两个电子而成为镁离子 化学反应前后元素的种类不变
分析:根据图示中原子变为离子后的情况分析解答即可;
解答:由图示可以看出化学反应中镁原子易失掉最外层的两个电子而成为镁离子,同时也可以看出镁离子带正电荷而原子不带电以及化学反应前后元素的种类不变等信息;
故答案为:化学反应中镁原子易失掉最外层的两个电子而成为镁离子;化学反应前后元素的种类不变;
点评:此题是对化学变化的微观情况的考查,解题的关键是对相关图示中合理信息的读取;
分析:根据图示中原子变为离子后的情况分析解答即可;
解答:由图示可以看出化学反应中镁原子易失掉最外层的两个电子而成为镁离子,同时也可以看出镁离子带正电荷而原子不带电以及化学反应前后元素的种类不变等信息;
故答案为:化学反应中镁原子易失掉最外层的两个电子而成为镁离子;化学反应前后元素的种类不变;
点评:此题是对化学变化的微观情况的考查,解题的关键是对相关图示中合理信息的读取;

练习册系列答案
相关题目
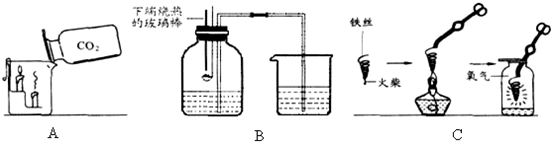

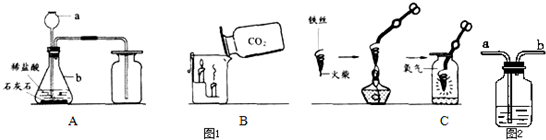
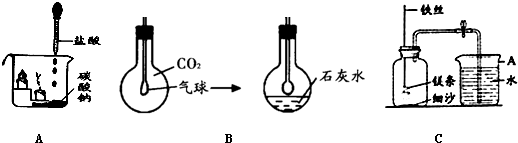
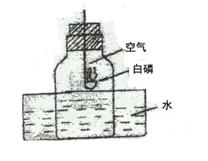 在燃烧匙上的足量白磷点燃后插入雪碧瓶中,塞紧瓶塞,观察至冷却。
在燃烧匙上的足量白磷点燃后插入雪碧瓶中,塞紧瓶塞,观察至冷却。
 ,
, 点燃后立即插入雪碧瓶中,塞紧瓶塞,发现镁条继续燃
点燃后立即插入雪碧瓶中,塞紧瓶塞,发现镁条继续燃