题目内容
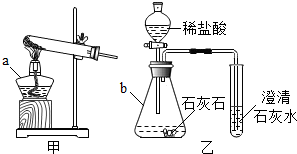
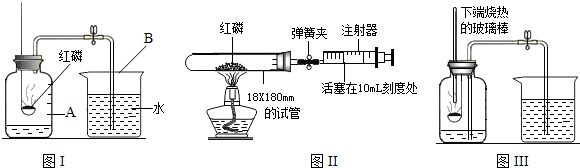
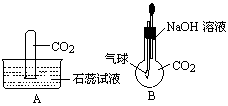
某化学兴趣小组用图中所示的装置做有关C02及镁条在空气中燃烧的实验.
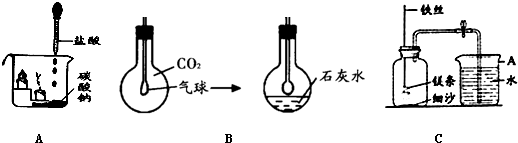
(1)实验探究:如上图A所示,向烧杯内碳酸钠粉末滴入盐酸,观察到烧杯中燃着的小蜡烛下面一支火焰先熄灭,上面一支随后熄灭.从这个实验可以得出的结论是:
①
②
③
(2)小军向烧瓶中倒入澄清石灰水(如B图所示),立即塞紧瓶塞,并轻轻振荡,
①可观察到:澄清石灰水变浑浊, ;
②产生另一现象的原因是: ;
(3)某校研究性学习小组用上图C装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
①如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的 %.
②现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中除了氧气和二氧化碳以外,还一定含有 .镁条还可以在二氧化碳气体中燃烧生成碳和氧化镁,该反应的化学方程式是 .

(1)实验探究:如上图A所示,向烧杯内碳酸钠粉末滴入盐酸,观察到烧杯中燃着的小蜡烛下面一支火焰先熄灭,上面一支随后熄灭.从这个实验可以得出的结论是:
①
②
③
(2)小军向烧瓶中倒入澄清石灰水(如B图所示),立即塞紧瓶塞,并轻轻振荡,
①可观察到:澄清石灰水变浑浊,
②产生另一现象的原因是:
(3)某校研究性学习小组用上图C装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
①如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的
②现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中除了氧气和二氧化碳以外,还一定含有
分析:(1)据所发生的反应以及蜡烛熄灭的顺序判断二氧化碳的物理性质和化学性质;
(2)二氧化碳与澄清石灰水可反应,可使瓶内气压变小,据此分析解答;
(3)①氧气约占空气体积分数的21%,而氮气占78%,从而可判断只消耗氧气时,气体减少原体积的21%;
②空气中氮气、氧气所占的体积分数是99%,气体减少达70%时,大部分气体被消耗,说明减少的气体已不完全为氧气了,还应消耗了氮气,氮气和镁在点燃条件下能生成氮化镁.
(2)二氧化碳与澄清石灰水可反应,可使瓶内气压变小,据此分析解答;
(3)①氧气约占空气体积分数的21%,而氮气占78%,从而可判断只消耗氧气时,气体减少原体积的21%;
②空气中氮气、氧气所占的体积分数是99%,气体减少达70%时,大部分气体被消耗,说明减少的气体已不完全为氧气了,还应消耗了氮气,氮气和镁在点燃条件下能生成氮化镁.
解答:解:(1)向烧杯内碳酸钠粉末滴入盐酸,观察到烧杯内燃着的小蜡烛下面一支火焰先熄灭,上面一支随后熄灭,所以可以判断碳酸钠可以和稀盐酸反应生成二氧化碳,同时也说明二氧化碳不燃烧也不支持燃烧,下面的蜡烛先熄灭,说明二氧化碳的密度比空气大;
(2)二氧化碳与澄清石灰水反应生成不溶于水的白色沉淀碳酸钙,使瓶内气压变小,大气压将空气压入气球,从而使气球胀大;
(3)①如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的21%;
②实验中进入瓶中水的体积达70%,说明反应消耗空气的体积为70%,因此已不是仅消耗氧气了,还应消耗部分氮气;镁条在氮气中燃烧的化学方程式为:N2+3Mg
Mg3N2;
故答案为:(1)①碳酸钠与盐酸反应生成CO2;
②CO2不燃烧,不支持燃烧;
③CO2密度比空气大.
(2)①气球胀大;
②二氧化碳与澄清石灰水反应,瓶内气压变小,大气压将空气压入气球,从而使气球胀大;
(3)①21%;
②氮气;N2+3Mg
Mg3N2.
(2)二氧化碳与澄清石灰水反应生成不溶于水的白色沉淀碳酸钙,使瓶内气压变小,大气压将空气压入气球,从而使气球胀大;
(3)①如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的21%;
②实验中进入瓶中水的体积达70%,说明反应消耗空气的体积为70%,因此已不是仅消耗氧气了,还应消耗部分氮气;镁条在氮气中燃烧的化学方程式为:N2+3Mg
| ||
故答案为:(1)①碳酸钠与盐酸反应生成CO2;
②CO2不燃烧,不支持燃烧;
③CO2密度比空气大.
(2)①气球胀大;
②二氧化碳与澄清石灰水反应,瓶内气压变小,大气压将空气压入气球,从而使气球胀大;
(3)①21%;
②氮气;N2+3Mg
| ||
点评:此题考察知识点的方式比较灵活,但并不是难题,同学们只要掌握二氧化碳的物理化学性质,了解空气组成成分,利用镁的性质及题中资料信息考查学生获得信息、解决问题的能力.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目