题目内容
【题目】己知某粗盐样品中含有Na2SO4、MgCl2、CaCl2等杂质,实验室提纯流程如下:
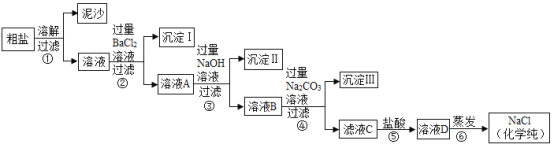
(1)沉淀Ⅱ的成分是___________(填化学式);
(2)第④步操作中加入过量Na2CO3溶液的目的是______
(3)现用提纯所得的固体氯化钠配制50g溶质质量分数为12%的氯化钠溶液,配制过程中需要用到的仪器除了量筒,烧杯,玻璃棒,药匙外,还需要______
(4)若用上述所的分数为12%的氯化钠溶液配制20g质量分数为6%的氯化钠溶液,需要水的体积为_____mL.(水的密度为1g/cm3)
【答案】Mg(OH)2 除去杂质CaCl2和加入的过量试剂BaCl2 托盘天平、胶头滴管 10
【解析】
(1)氢氧化钠和氯化镁反应会生成氯化钠和氢氧化镁沉淀,所以沉淀Ⅱ的成分是:Mg(OH)2;
(2)碳酸钠和氯化钙反应会生成碳酸钙沉淀和氯化钠,和氯化钡反应会生成碳酸钡沉淀和氯化钠,所以第④步操作中加入过量Na2CO3,溶液的目的是:除去杂质CaCl2和加入的过量试剂BaCl2;
(3)配制过程中需要用到的仪器除了量筒、烧杯、玻璃棒、药匙外,还需要托盘天平、胶头滴管;
(4)溶液稀释前后,溶质质量不变,所以需要水的质量为:![]() -10g=10g,体积为10mL。
-10g=10g,体积为10mL。
故答案为:(1)Mg(OH)2;
(2)除去杂质CaCl2和加入的过量试剂BaCl2;
(3)托盘天平、胶头滴管;
(4)10。

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目