题目内容
【题目】质量守恒定律的发现对化学的发展作出了重要贡献.
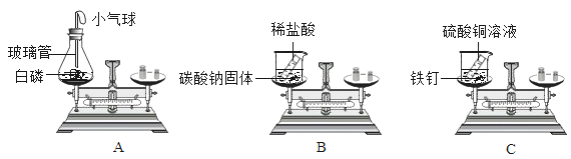
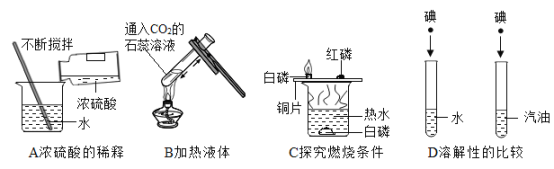
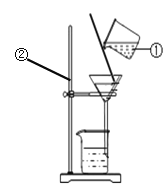
(1)用如图所示的3个实验验证质量守恒定律,其中实验前后天平不能保持平衡的是_____ (填序号),理由是_____
(2)从微观角度分析有助于我们理解质量守恒定律.在一密闭容器内有4种物质A、B、C、D,它们在一定条件下发生化学反应。经过一段时间后停止反应,其中A、B、C、D的微观示意图和反应前后各物质的质量如下表所示。
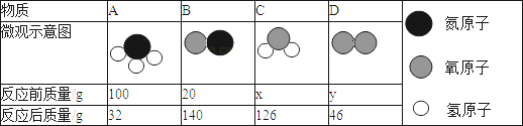
(Ⅰ)从微观角度分析,化学反应中质量守恒的原因是_____
(Ⅱ)B的化学式为_____。
(Ⅲ)该反应中B和C的质量比为_____。
(Ⅳ)表中x的值是_____
【答案】B 装置未密闭,生成的二氧化碳气体逸出,导致左盘中容器内的物质总质量减少 化学反应前后原子的种类不变,原子的数目不变,原子的质量不变 NO 10∶9 18
【解析】
(1)分析三个实验可以知道,A中反应是在密闭的容器中进行,反应前后物质的总质量不变;B装置未密闭,生成的二氧化碳气体逸出,导致左盘中容器内的物质总质量减少;C虽然是敞口的容器中反应但是没有生成气体也没有空气中的成分参与反应,反应前后物质的总质量也不变。因此可以判断B实验前后天平不能保持平衡。故选B。
(2)Ⅰ、根据化学反应的实质可以知道,在反应的过程中是分子裂解成原子,原子进行了重新组合而得到新的分子,所以该过程中原子的种类、原子的数目和原子的质量都没有发生改变,所以化学反应前后质量守恒。
Ⅱ、根据题中的图例可以知道B物质的一个分子是由一个氮原子和一个氧原子组成的,所以该物质的化学式为:NO。
Ⅲ、根据表格中的信息可以知道,反应前后B的质量增加了,所以B为生成物,而反应前后A物质的质量减少了,所以A为反应物,结合反应前后元素的种类不变可以知道,反应物为A和D,而生成物为B和C,其中A为NH3 ,B为NO,C为H2O,D为O2,所以可以写出该反应的化学方程式为: ;反应中物质的质量比等于它们的相对分子质量乘以化学计量数的比,所以可以知道B和C的质量比=120∶108=10∶9;
;反应中物质的质量比等于它们的相对分子质量乘以化学计量数的比,所以可以知道B和C的质量比=120∶108=10∶9;
Ⅳ、根据Ⅲ的解答可以知道,反应中生成B的质量为:140g﹣20g=120g,而B∶C=10∶9,所以可以判断反应中生成C的质量为108g,即126﹣x=108,所以x=18。

 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案