题目内容
【题目】图中甲是元素周期表中硒元素的部分信息,乙是硒元素的原子结构示意图。据图回答问题:
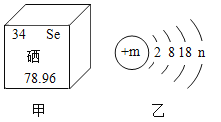
(1)硒元素位于周期表中的第_______周期。
(2)图乙中m表示________,m的值为_________,n的值为_____________。
(3)硒元素属于_____________元素(填“金属”或“非金属”);硒元素的相对原子质量为______。
(4)当n=8时,该粒子带有____________个单位的负电荷。
【答案】4 核内质子数 34 6 非金属 78.96 2
【解析】
(1)周期数=原子核外电子层数,硒元素的原子核外有4个电子层,则在元素周期表中,硒元素位于第4周期;
(2)图乙中m表示核内质子数;根据元素周期表中的一格可知,左上角的数字为34,表示原子序数为34;根据原子中原子序数=核电荷数=质子数=核外电子数,则该元素的原子核内质子数和核外电子数为34;34=2+8+18+n,n=6;
(3)硒带“石”字旁,属于固态非金属元素;根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为78.96;
(4)当 n=8时,质子数=34,核外电子数=36,质子数<核外电子数,该粒子带有2个单位的负电荷。

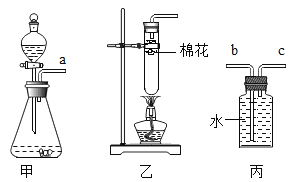
【题目】下列实验指定容器中的水,其解释没有体现水的主要作用的是( )
A | B | C | D | |
实 验 装 置 |
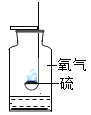
硫在氧气中燃烧 |
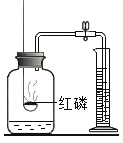
测定空气中氧气含量 |
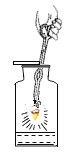
铁丝在氧气中燃烧 |
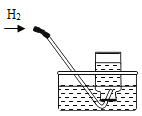
排水法收集氢气 (氢气难溶于水) |
解释 | 集气瓶中的水:吸收放出的热量 | 量筒中的水:通过水体积的变化得出O2体积 | 集气瓶中的水:冷却溅落融熔物,防止集气瓶炸裂 | 集气瓶中的水:水先将集气瓶内的空气排净,后便于观察氢气何时收集满 |
A.AB.BC.CD.D
【题目】同一个化学反应在不同条件下反应的快慢(即反应速率)是不同的。下列三组实验是探究不同条件对金属锌与盐酸反应速率的影响
实验操作 | 现象 | 结论 | |
第1组 |
| ①(选填“锌粒”或“锌粉”)反应更加剧烈。 | 反应物表面积越大,反应速率越大。 |
第2组 |
| 锌粒与20%的盐酸反应更加剧烈。 | 反应物② 越大,反应速率越大。 |
第3组 |
| 置于热水的试管反应更加剧烈。 | 温度越高,反应的速率越大。 |
(1)将表中的空格填写完整①_________②_________③__________
(2)请写出锌与稀盐酸反应的化学方程式_______________
(3)为了提高铁与盐酸反应的反应速率,请提出一种实验方案_____________
(4)综合其它实验结果,相同质量的铁、锌、铜与足量的稀盐酸反应产生氢气的质量关系如下图,其中正确的是__________(填选项)