��Ŀ����
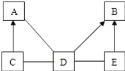
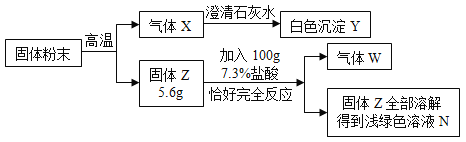
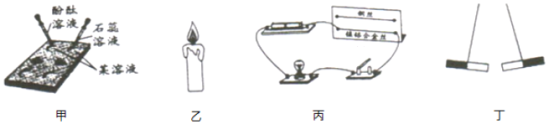
����Ŀ��ij��ɫ����A���ܺ���̼���ơ������ơ��Ȼ��ơ����ᱵ�е�һ�ֻ��֣���������ʵ�飺(��Ϣ��ʾ�������ơ����ᱵ��Һ������)
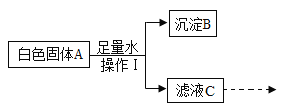
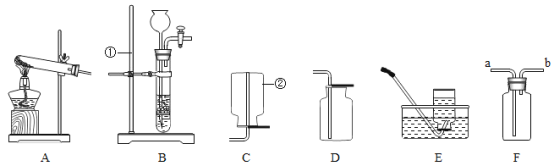
�ٲ���I��____��
���ڳ���B�м�������ϡ���ᣬ���������ܽ⣮��������ʵ�������A��һ�����е�������_____��д�����������ܽ�Ļ�ѧ����ʽ____��
��ȡ������ҺC���Թ��У������̪����Һ��죬��C��һ�����е�������____��
��Ϊ��һ��ȷ������A�п��ܴ��ڵ����ʣ�����ҺC����ʵ�飬����±���
ʵ����� | ���� | ���� |
____ | ____ | ȷ��A�����л������Ȼ��� |
���𰸡����� Na2CO3��Na2SO4��Ba(NO3)2 BaCO3+2HNO3=Ba(NO3)2+H2O+CO2�� NaNO3��Na2CO3 ȡ��ҺC��������������Ba(NO3)2��Һ�����˺�����Һ�е���AgNO3��Һ ������ɫ����
��������
�ٲ���I�ǽ������Һ����룬���ڹ��˲�����
��������ȷ��ij��ɫ������ܺ����Ȼ��ơ������ơ�̼���ơ����ᱵһ�ֻ��֣�����ͼ�г��������Ʋ������̼�ᱵ�����ᱵ�������������ڳ���B�м�������ϡ���ᣬ���������ܽ��������Ʋ����Ϊ̼�ᱵ�����Ʋ�һ�����е�����Na2CO3��Na2SO4��Ba(NO3)2��̼�ᱵ��ϡ���ᷴӦ�������ᱵ��ˮ�Ͷ�����̼��
�������ƺ����ᱵ��Ӧ�������ᱵ�������ƣ�̼���ƺ����ᱵ��Ӧ����̼�ᱵ�������ƣ�������ȡ������ҺC���Թ��У������̪����Һ��죬���Ʋ�̼���ƹ��������NaNO3��Na2CO3��
�ܸ����������������ӽ�������Ȼ��������������ʵ��Կ��ܴ��ڵ����ʼ������𣬲���Ϊ����ȡԭ���������Һ������������ᱵ��Һ�����ˣ��ټ�����������Һ��ϡ��������������������Ȼ��ƣ����ޣ���û���Ȼ��ƣ�
�ʴ�Ϊ��
�ٹ��ˣ���Na2CO3��Na2SO4��Ba��NO3��2��BaCO3+2HNO3=Ba��NO3��2+H2O+CO2����
��NaNO3��Na2CO3����
ʵ����� | ���� | ���� |
ȡ��ҺC��������������Ba��NO3��2��Һ�����˺�����Һ�е���AgNO3��Һ | ������ɫ���� |

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ��ͼ�����Ӧ�ı���һ�µ���
ʵ�� | x���ʾ�ĺ��� | y���ʾ�ĺ��� | |
A | ��MnO2����˫��ˮ�� | ʱ�䣨s�� | ��Һ��ˮ��������g�� |
B | ����������װ�п������ܱյļ���ƿ��ȼ�� | ʱ�䣨s�� | ƿ������������mL�� |
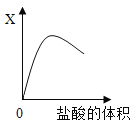
C | ���ɫ����ͭ��ĩ����εμ�ˮ | ˮ��������g�� | ��Һ��������g�� |
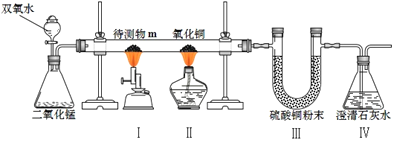
D | CO��CuO��Ӧ | ͨ��CO�����ʵ�����mol�� | CuO�����ʵ�����mol�� |
A. 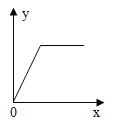 �������̷���˫��ˮ��
�������̷���˫��ˮ��
B. 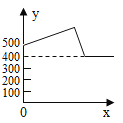 ����������װ�п������ܱռ���ƿ��ȼ��
����������װ�п������ܱռ���ƿ��ȼ��
C. 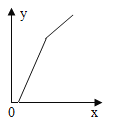 ��ɫ����ͭ��ĩ����εμ�ˮ
��ɫ����ͭ��ĩ����εμ�ˮ
D. 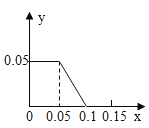 COͨ�����ȵ�CuO
COͨ�����ȵ�CuO