题目内容
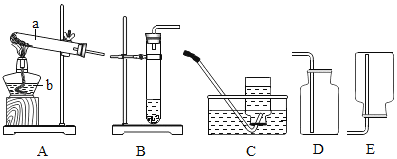
【题目】某兴趣小组为探究化合物m(可能含碳、氢元素)的组成进行实验(装置气密性良好):通一段时间氧气后点燃酒精喷灯与酒精灯。待完全反应完成后,先熄灭火源,再停止通入氧气。
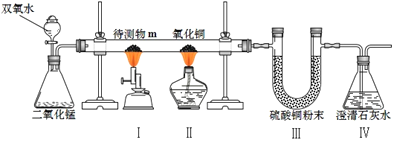

如图是某同学记录的部分实验现象。请回答
①装置Ⅲ中发生反应的化学方程式_____。
②现象_____(填序号说明化合物m中有碳元素存在。
③你认为该实验是否需要尾气处理,并说明理由_____。
④若要确定混合物m中是否含有氢元素,需要对装置进行的改进是_____。
【答案】CuSO4+5H2O=CuSO4·5H2O Ⅳ 不需要,通过氧化铜无变化说明没有有毒气体一氧化碳生成。(合理给分) 在装置Ⅰ之前添加一个干燥装置
【解析】
①无水硫酸铜遇水变蓝,装置Ⅲ中硫酸铜粉末由白色变为蓝色,说明化合物m加热有水生成,说明化合物m中有氢元素存在.发生反应的化学方程式为:CuSO4+5H2O═CuSO45H2O;
②二氧化碳能使澄清的石灰水变浑浊,Ⅳ中澄清的石灰水变浑浊,说明化合物m加热有二氧化碳生成,根据质量守恒定律,说明化合物m中有碳元素存在.
③根据题中信息可知:加热氧化铜始终无变化,说明没有有毒气体一氧化碳生成,不需要尾气处理;
④用过氧化氢溶液和二氧化锰制氧气时,氧气中可能混有水分,为排除水分对确定混合物m中是否含有氢元素的干扰,需要对装置进行的改进是在装置Ⅰ之前添加一个干燥装置.
答案:
①CuSO4+5H2O═CuSO45H2O;
②Ⅳ;
③不需要,通过氧化铜无变化说明没有有毒气体一氧化碳生成.(合理给分)
④在装置Ⅰ之前添加一个干燥装置.

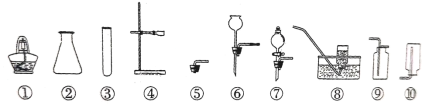
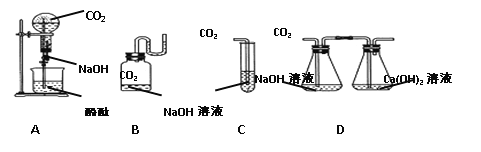
【题目】氯气(Cl2)是黄绿色气体,氯气溶于水部分以Cl2分子存在于溶液中,部分与水反应Cl2+H2O=HCl+HClO.产物中,次氯酸HClO是一种弱酸.氯气溶于水所得溶液称为氯水.把品红试纸(染有品红颜料的滤纸)放入氯水中,品红试纸褪色.如图是实验室制取氯气的成套装置图,请填空:

(1)仪器X的名称是:_____.
(2)从反应物的状态和反应条件看,装置甲属于_____型气体发生装置.
(3)氯气在装置丁中被收集,其收集方法为_____,装置戊中可得到氯水.
(4)晓红对“氯水使品红试纸褪色”产生兴趣,她所在的学习小组进行了如下探究,请你一起来完成:
(提出问题)氯水中的什么成分使品红试纸褪色?
(猜 想)猜想1:氯水中的水使品红试纸褪色;
猜想2:氯水中的Cl2使品红试纸褪色;
猜想3:氯水中的盐酸使品红试纸褪色;猜想4:氯水中的_____(填化学式)使品红试纸褪色.
(实验探究)
实 验 操 作 | 实 验 现 象 | 结 论 |
①把品红试纸放入水中 | _____ | 猜想1不成立 |
②把品红试纸放入干燥的氯气中 | 试纸不褪色 | 猜想2不成立 |
③_____ | 试纸不褪色 | 猜想3不成立 |
(结 论)学习小组通过讨论,找到了氯水中使品红试纸褪色的物质.
(反 思)向氯水中滴加几滴紫色石蕊试液,会观察到的现象是_____.
【题目】稀盐酸与氢氧化钠溶液混合后,发现溶液仍为无色。为了证明她们确实发生了化学反应,某学习小组进行如下实验:
|
|
图1 | 图2 |
| |
图3 | |
① 图1中从a→b整个实验过程中观察到的现象是_________________,由此证明上述实验过程确实发生了化学反应。
② 图2表示反应过程中溶液的PH变化情况,c点表示的意义是________________;当溶液的pH=2时,此溶液的溶质有_______________。
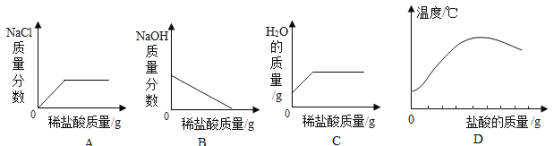
③ 图3表示向一定量的氢氧化钠溶液中逐滴加入稀盐酸至过量,图像中能正确反应对应变化关系的是________________。
④ 为测定氢氧化钠溶液的质量分数,取氢氧化钠溶液50g,用10%的稀盐酸进行测定,当加入稀盐酸为36.5g时恰好完全反应。
I. 稀盐酸中含HCl的物质的量是_____mol;
II. 氢氧化钠溶液的质量分数是___________。(根据化学方程式列式计算)