题目内容
【题目】下图是实验室常用的实验仪器与装置,回答下列问题。
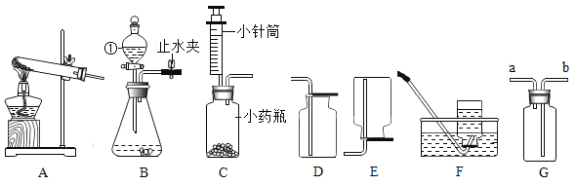
(1)图中仪器的名称:①____②____
(2)实验室用高锰酸钾制取并收集一瓶较为纯净的氧气,仪器的组合为(填装置序号)____,反应的化学方程式为___。
(3) 实验室常用装置B制取二氧化碳,常用的药品是___(填名称),其反应的化学方程式为____,某同学利用生活中的物品设计图C装置,该装置与B相比其优点是____,小注射器的作用相当于实验室中的____(填仪器名称)。
(4)关闭B装置中的止水夹后,从长颈漏斗向锥形瓶中注入一定量的水,静止后如图所示,则B装置____(填“漏气”、“不漏气”或“无法确定”);
(5)实验室常用醋酸钠固体和碱石灰固体混合加热制备甲烷(CH4)气体,发生装置应选用___,已知甲烷密度比空气小,如用G装置来收集,甲烷应从___(a或b)通入。
(6)二氧化碳的水溶液能使蓝色石蕊试纸变红,若用装置H证明使蓝色石蕊试纸变红的物质是碳酸而不是水或二氧化碳,应该采取的实验操作顺序是___(填字母代号)。
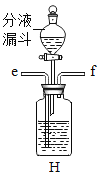
①从f端通氮气 ②从分液漏斗中滴加适量水 ③从e端通二氧化碳 ④将干燥的蓝色石蕊试纸放入H装置的广口瓶中
A ④③①②③ B ③④②①③ C ④②③①③
【答案】长颈漏斗 水槽 AF 2KMnO4![]() K2MnO4+MnO2+O2↑ 石灰石(或大理石)和稀盐酸 CaCO3+2HCl=CaCl2+H2O+CO2↑ 能控制反应速率 分液漏斗 不漏气 A b A
K2MnO4+MnO2+O2↑ 石灰石(或大理石)和稀盐酸 CaCO3+2HCl=CaCl2+H2O+CO2↑ 能控制反应速率 分液漏斗 不漏气 A b A
【解析】
(1)图中仪器的名称:①长颈漏斗,②水槽。
(2)实验室用高锰酸钾制取并收集一瓶较为纯净的氧气,该反应属于固体加热型,排水法收集的氧气较为纯净,仪器的组合为AF,加热高锰酸钾反应生成锰酸钾、二氧化锰和氧气,反应的化学方程式为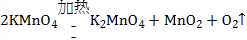 。
。
(3) 实验室常用装置B制取二氧化碳,常用的药品是石灰石(或大理石)和稀盐酸,碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为![]() ,某同学利用生活中的物品设计图C装置,该装置与B相比其优点是能控制反应速率,小注射器的作用相当于实验室中的分液漏斗。
,某同学利用生活中的物品设计图C装置,该装置与B相比其优点是能控制反应速率,小注射器的作用相当于实验室中的分液漏斗。
(4)关闭B装置中的止水夹后,从长颈漏斗向锥形瓶中注入一定量的水,静止后如图所示,则B装置不漏气;
(5)实验室常用醋酸钠固体和碱石灰固体混合加热制备甲烷气体,发生装置应选用A,已知甲烷密度比空气小,如用G装置来收集,甲烷应从b通入。
(6)二氧化碳的水溶液能使蓝色石蕊试纸变红,若用装置H证明使蓝色石蕊试纸变红的物质是碳酸而不是水或二氧化碳,应该采取的实验操作顺序是:
④将干燥的蓝色石蕊试纸放入H装置的广口瓶中;
③从e端通二氧化碳(检验二氧化碳能否使蓝色石蕊试纸变红);
①从f端通氮气(除尽装置中的二氧化碳);
②从分液漏斗中滴加适量水(检验水能否使蓝色石蕊试纸变红);
③从e端通二氧化碳(验证二氧化碳的水溶液能使蓝色石蕊试纸变红);
故填:A。

【题目】一定条件下,在密闭容器内投入SO2、O2、SO3、V2O5四种物质,发生反应的化学方程式为2SO2+O2![]() 2SO3。在不同时刻测得容器内各物质的质量如下表所示,下列说法不正确的是
2SO3。在不同时刻测得容器内各物质的质量如下表所示,下列说法不正确的是
物质 | 甲 | 乙 | 丙 | 丁 |
t1 | 80g | 5g | 100g | 5g |
t2 | a | 55g | 60g | b |
t3 | c | d | 40g | 5g |
A.甲是O2,丁是V2O5
B.a = 70g,d = 25g
C.参加反应的SO2、O2的分子个数比为2︰1
D.参加反应的SO2、O2的质量比为4︰1