题目内容
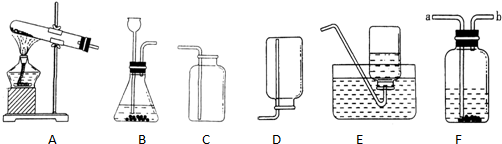
如图所示某同学探究Fe、Cu、Ag三种金属活动性顺序的一组实验,你认为(填能或不能)达到实验目的,如果认为不能,请你在此基础上补充一个实验,帮助这位同学达到实验目的(说明实验步骤、现象、结论).
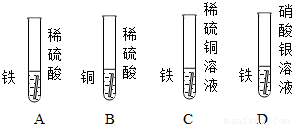
【答案】分析:通过对比AB选项可以得出铁比铜的活动性强,C选项得出的结论同上,D选项可以得出铁比银的活动性强,但全部选项不能得出铜和银的活动性强弱比较.
解答:解:AB选项和C选项都可以得出铁比铜活泼,D选项可以得出铁比银活泼,全部选项不能得出铜和银的活动性强弱比较,所以需要补充实验验证铜和银的活动性.故答案为:
不能;
把铜置于硝酸银溶液中,铜的表面有白色固体生成,说明铜的活动性比银强.
点评:主要通过金属与酸,金属与盐的反应考查了金属活动性的应用,所以还是要熟练掌握金属的性质.
解答:解:AB选项和C选项都可以得出铁比铜活泼,D选项可以得出铁比银活泼,全部选项不能得出铜和银的活动性强弱比较,所以需要补充实验验证铜和银的活动性.故答案为:
不能;
把铜置于硝酸银溶液中,铜的表面有白色固体生成,说明铜的活动性比银强.
点评:主要通过金属与酸,金属与盐的反应考查了金属活动性的应用,所以还是要熟练掌握金属的性质.

练习册系列答案
相关题目
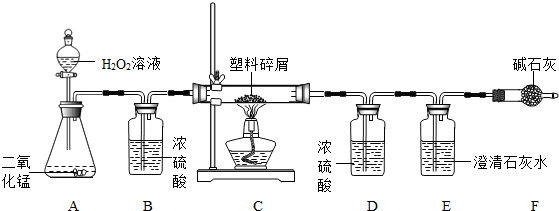
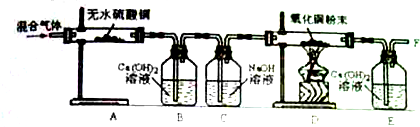
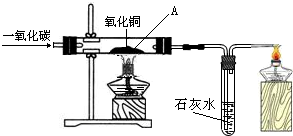 (2009?武威)如图所示,某同学用一氧化碳代替氢气还原氧化铜制取金属铜.请你参与他的探究过程,并回答下列问题.
(2009?武威)如图所示,某同学用一氧化碳代替氢气还原氧化铜制取金属铜.请你参与他的探究过程,并回答下列问题.