题目内容
(2010?新乡一模)当矿井内遇有灾害事故,造成环境中缺氧或出现高浓度有毒有害气体时,可佩戴“化学氧自救器”逃生.其化学反应原理为:正常呼气时,呼出的二氧化碳气体和药罐内生氧剂(过氧化钠Na2O2)发生化学反应产生氧气以供给人呼吸.某化学活动小组的同学围绕其化学反应原理进行了一系列的探究活动.
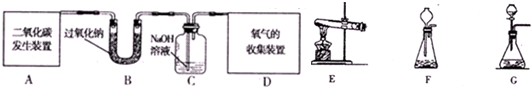
(1)用如图所示由A、B、C、D组合成的成套装置和有关药品制取并收集氧气.
①若用石灰石与稀酸盐反应制取二氧化碳,则A装置可采用下图中的
②用C装置中的氢氧化钠溶液吸收未与过氧化钠反应的二氧化碳.请写出氢氧化钠与二氧化碳反应的化学方程式
③证明生成的气体是氧气,可使用
(2)二氧化碳与过氧化钠反应除生成氧气还生成什么其他物质?有位同学推测可能生成了一种酸或一种碱,另一个同学认为不可能,其理由是
(3)有同学推测可能生成了一种碳酸盐.并设计了以下实验进行验证,请将下表填写完整.
(4)如果每人每小时消耗的氧气在某温度和压强条件下的体积为50L,若从矿井中逃生需2小时,则“化学氧自救器”中至少需要过氧化钠多少克?(已知:在上述温度和压强条件下氧气的密度为1.5g/L)

(1)用如图所示由A、B、C、D组合成的成套装置和有关药品制取并收集氧气.
①若用石灰石与稀酸盐反应制取二氧化碳,则A装置可采用下图中的
F或G
F或G
(填序号)有关反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
.②用C装置中的氢氧化钠溶液吸收未与过氧化钠反应的二氧化碳.请写出氢氧化钠与二氧化碳反应的化学方程式
2NaOH+CO2 =Na2CO3+H2O
2NaOH+CO2 =Na2CO3+H2O
.③证明生成的气体是氧气,可使用
带火星的木条
带火星的木条
进行检验.(2)二氧化碳与过氧化钠反应除生成氧气还生成什么其他物质?有位同学推测可能生成了一种酸或一种碱,另一个同学认为不可能,其理由是
二氧化碳与过氧化钠都不含氢元素,故不可能生成含有氢元素的酸或碱
二氧化碳与过氧化钠都不含氢元素,故不可能生成含有氢元素的酸或碱
.(3)有同学推测可能生成了一种碳酸盐.并设计了以下实验进行验证,请将下表填写完整.
| 实验步骤 | 实验现象 | 实验结论 |
| 将二氧化碳与过氧化钠反应后的固体 加入一只小试管中,然后滴加适量的稀盐酸,再把生成的气体通入澄清的石灰水 加入一只小试管中,然后滴加适量的稀盐酸,再把生成的气体通入澄清的石灰水 |
试管中有气泡冒出,澄清的石灰水变浑浊 试管中有气泡冒出,澄清的石灰水变浑浊 |
二氧化碳与过氧化钠反应生成的化合物是 碳酸盐 碳酸盐 |
分析:(1)①发生装置主要由反应物的状态和反应条件决定;根据反应物、生成物以及反应条件正确书写化学方程式;
②氢氧化钠与二氧化碳反应生成碳酸钠和水,据此书写化学反应方程式;
③根据氧气能支持燃烧的性质,可以用带火星的木条进行检验;
(2)根据质量守恒定律可以知道反应前后元素的种类不变,对作出的猜想做出合理的判断与解释;
(3)要验证该反应可能生成了一种碳酸盐,只要用稀盐酸和澄清的石灰水验证碳酸根离子的存在就可以了.
(4)根据化学方程式的计算解决,先要对消耗的氧气进行体积与质量的转化,再利用2Na2O2+2CO2=2Na2CO3+O2↑求过氧化钠的质量.
②氢氧化钠与二氧化碳反应生成碳酸钠和水,据此书写化学反应方程式;
③根据氧气能支持燃烧的性质,可以用带火星的木条进行检验;
(2)根据质量守恒定律可以知道反应前后元素的种类不变,对作出的猜想做出合理的判断与解释;
(3)要验证该反应可能生成了一种碳酸盐,只要用稀盐酸和澄清的石灰水验证碳酸根离子的存在就可以了.
(4)根据化学方程式的计算解决,先要对消耗的氧气进行体积与质量的转化,再利用2Na2O2+2CO2=2Na2CO3+O2↑求过氧化钠的质量.
解答:解:(1)①反应物的状态是固态和液态,反应条件是常温,应选固-液不加热型的发生装置F或G;石灰石的主要成份是碳酸钙,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳;其反应方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑.
故答案为:F或G;CaCO3+2HCl=CaCl2+H2O+CO2↑;
②氢氧化钠和二氧化碳反应生成碳酸钠和水,其反应方程式是:2NaOH+CO2 =Na2CO3+H2O.
故答案为:2NaOH+CO2 =Na2CO3+H2O;
③检验是否是氧气用的是带火星的木条.将带火星的木条伸入盛有气体的集气瓶内观察,如木条复燃就证明是氧气.
故答案是:带火星的木条;
(2)根据质量守恒定律可以知道:二氧化碳与过氧化钠都不含氢元素,故不可能生成含有氢元素的酸或碱.
故答案是:二氧化碳与过氧化钠都不含氢元素,故不可能生成含有氢元素的酸或碱;
(3)为了验证该反应可能生成了一种碳酸盐,只要验证生成物中有碳酸根就可以了,因此需要用两种试剂稀盐酸和澄清的石灰水.
故答案是:加入一只小试管中,然后滴加适量的稀盐酸,再把生成的气体通入澄清的石灰水;试管中有气泡冒出,澄清的石灰水变浑浊;碳酸盐;
(4)50L氧气的质量为:50L×1.5g/L=75g
该潜水艇中每天消耗氧气的质量为:2×75g=150g,
设该潜水艇中2小时需要过氧化钠的质量为x.
2Na2O2+2CO2=2Na2CO3+O2↑
156 32
x 150g
则
=
,
解得,x=731.25g.
答:“化学氧自救器”中至少需要过氧化钠731.5克.
故答案为:F或G;CaCO3+2HCl=CaCl2+H2O+CO2↑;
②氢氧化钠和二氧化碳反应生成碳酸钠和水,其反应方程式是:2NaOH+CO2 =Na2CO3+H2O.
故答案为:2NaOH+CO2 =Na2CO3+H2O;
③检验是否是氧气用的是带火星的木条.将带火星的木条伸入盛有气体的集气瓶内观察,如木条复燃就证明是氧气.
故答案是:带火星的木条;
(2)根据质量守恒定律可以知道:二氧化碳与过氧化钠都不含氢元素,故不可能生成含有氢元素的酸或碱.
故答案是:二氧化碳与过氧化钠都不含氢元素,故不可能生成含有氢元素的酸或碱;
(3)为了验证该反应可能生成了一种碳酸盐,只要验证生成物中有碳酸根就可以了,因此需要用两种试剂稀盐酸和澄清的石灰水.
故答案是:加入一只小试管中,然后滴加适量的稀盐酸,再把生成的气体通入澄清的石灰水;试管中有气泡冒出,澄清的石灰水变浑浊;碳酸盐;
(4)50L氧气的质量为:50L×1.5g/L=75g
该潜水艇中每天消耗氧气的质量为:2×75g=150g,
设该潜水艇中2小时需要过氧化钠的质量为x.
2Na2O2+2CO2=2Na2CO3+O2↑
156 32
x 150g
则
| 156 |
| x |
| 32 |
| 150 |
解得,x=731.25g.
答:“化学氧自救器”中至少需要过氧化钠731.5克.
点评:本道题目看起来比较麻烦,但实际考查的是二氧化碳发生装置的选择、实验室制二氧化碳的原理方程式、碳酸根的检验等一些基础性知识.另外根据化学式计算,主要考查计算的方法和计算的准确性.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目