题目内容
(2012?静安区一模)有一混合气体成分中可能含有水蒸气、一氧化碳、二氧化碳,某同学设计了如图所示实验装置探究混合气体的成分.
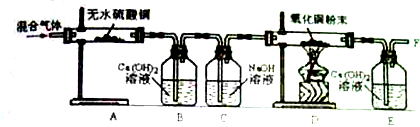
①实验中,若A装置中无水硫酸铜粉末有白色变为蓝色,证明混合气体中含有水蒸气,该反应的化学方程式
②若B中出现
③证明混合气体中含有一氧化碳的反应现象是
④装置C中氢氧化钠的作用是
⑤若混合气体中含有CO,在F处缺少的实验仪器或采取的措施
⑥如果将上述装置中的A、B交换,则不能能够检验混合气体中是否含有

①实验中,若A装置中无水硫酸铜粉末有白色变为蓝色,证明混合气体中含有水蒸气,该反应的化学方程式
CuSO4+5H2O═CuSO4?5H2O
CuSO4+5H2O═CuSO4?5H2O
②若B中出现
浑浊
浑浊
现象,则证明混合气体中含有二氧化碳,二氧化碳和石灰水反应的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O
Ca(OH)2+CO2═CaCO3↓+H2O
③证明混合气体中含有一氧化碳的反应现象是
D中黑色粉末变成红色
D中黑色粉末变成红色
、E中澄清石灰水变浑浊
E中澄清石灰水变浑浊
④装置C中氢氧化钠的作用是
吸收二氧化碳
吸收二氧化碳
⑤若混合气体中含有CO,在F处缺少的实验仪器或采取的措施
用酒精灯将剩余的一氧化碳燃烧掉
用酒精灯将剩余的一氧化碳燃烧掉
⑥如果将上述装置中的A、B交换,则不能能够检验混合气体中是否含有
水蒸气
水蒸气
.分析:①根据水和硫酸铜反应会生成蓝色的五水硫酸铜晶体进行解答;
②根据二氧化碳能使澄清石灰水变浑浊进行解答;
③根据一氧化碳具有还原性,能和氧化铜反应生成红色的铜和二氧化碳气体,二氧化碳能使澄清石灰水变浑浊进行解答;
④根据二氧化碳和氢氧化钠溶液反应生成碳酸钠和水进行解答;
⑤根据一氧化碳有毒进行解答;
⑥根据将上述装置中的A、B交换,气体先经过石灰水,所以不能能够检验混合气体中是否含有水蒸气进行解答.
②根据二氧化碳能使澄清石灰水变浑浊进行解答;
③根据一氧化碳具有还原性,能和氧化铜反应生成红色的铜和二氧化碳气体,二氧化碳能使澄清石灰水变浑浊进行解答;
④根据二氧化碳和氢氧化钠溶液反应生成碳酸钠和水进行解答;
⑤根据一氧化碳有毒进行解答;
⑥根据将上述装置中的A、B交换,气体先经过石灰水,所以不能能够检验混合气体中是否含有水蒸气进行解答.
解答:解:①水和硫酸铜反应会生成蓝色的五水硫酸铜晶体,该反应的化学方程式CuSO4+5H2O═CuSO4?5H2O;
故填:CuSO4+5H2O═CuSO4?5H2O;
②二氧化碳能使澄清石灰水变浑浊,所以若B中出现浑浊现象,则证明混合气体中含有二氧化碳,二氧化碳和石灰水反应的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O;
故填:浑浊;Ca(OH)2+CO2═CaCO3↓+H2O;
③一氧化碳具有还原性,能和氧化铜反应生成红色的铜和二氧化碳气体,二氧化碳能使澄清石灰水变浑浊,所以证明混合气体中含有一氧化碳的反应现象是D中黑色粉末变成红色,E中澄清石灰水变浑浊;
故填:D中黑色粉末变成红色;E中澄清石灰水变浑浊;
④二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,二氧化碳如果剩余会对一氧化碳的验证产生干扰,所以装置C中氢氧化钠的作用是吸收二氧化碳;
故填:吸收二氧化碳;
⑤若混合气体中含有CO,则未能与氧化铜反应的一氧化碳会直接排到空气中造成污染,因此,应在装置F处添置一酒精灯,把尾气中有毒的一氧化碳燃烧掉;
故填:用酒精灯将剩余的一氧化碳燃烧掉;
⑥若将装置A、B互换,混合气体首先通入澄清石灰水,不影响混合气体中二氧化碳的检验,但通过澄清石灰水的混合气体中一定会含有水,因此通过无色硫酸铜时变成的蓝色却不能说明原混合气体中是否含有水,或者说使无色硫酸铜变蓝色的水是还是澄清石灰水还是来自原混合气体将得不到说明,因此互换后不能检验混合气体中是否含有水蒸气.
故填:水蒸气.
故填:CuSO4+5H2O═CuSO4?5H2O;
②二氧化碳能使澄清石灰水变浑浊,所以若B中出现浑浊现象,则证明混合气体中含有二氧化碳,二氧化碳和石灰水反应的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O;
故填:浑浊;Ca(OH)2+CO2═CaCO3↓+H2O;
③一氧化碳具有还原性,能和氧化铜反应生成红色的铜和二氧化碳气体,二氧化碳能使澄清石灰水变浑浊,所以证明混合气体中含有一氧化碳的反应现象是D中黑色粉末变成红色,E中澄清石灰水变浑浊;
故填:D中黑色粉末变成红色;E中澄清石灰水变浑浊;
④二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,二氧化碳如果剩余会对一氧化碳的验证产生干扰,所以装置C中氢氧化钠的作用是吸收二氧化碳;
故填:吸收二氧化碳;
⑤若混合气体中含有CO,则未能与氧化铜反应的一氧化碳会直接排到空气中造成污染,因此,应在装置F处添置一酒精灯,把尾气中有毒的一氧化碳燃烧掉;
故填:用酒精灯将剩余的一氧化碳燃烧掉;
⑥若将装置A、B互换,混合气体首先通入澄清石灰水,不影响混合气体中二氧化碳的检验,但通过澄清石灰水的混合气体中一定会含有水,因此通过无色硫酸铜时变成的蓝色却不能说明原混合气体中是否含有水,或者说使无色硫酸铜变蓝色的水是还是澄清石灰水还是来自原混合气体将得不到说明,因此互换后不能检验混合气体中是否含有水蒸气.
故填:水蒸气.
点评:本题以实验探究的形式考查常见气体一氧化碳、二氧化碳和水蒸气的性质,解题的关键是根据实验装置图结合实验的目的分析各处装置在实验中的作用,要求同学们要具有综合的化学知识才能做好此题.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
