题目内容
化学实验是学习化学的基础,请根据下列装置图回答问题.
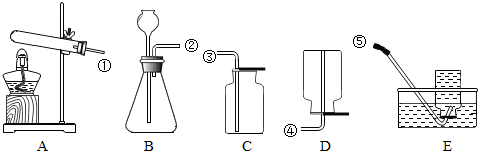
(1)装置E由导管、
(2)实验室用高锰酸钾加热制取氧气时,选用的发生装置是
用高锰酸钾制取氧气的文字表达式为
(3)若要收集一瓶较纯净的氧气应选择的收集装置是
(4)二氧化碳是一种无色、能溶于水且密度比空气大的气体;可选用的收集装置是

(1)装置E由导管、
集气瓶
集气瓶
和水槽
水槽
(填仪器名称)组成.(2)实验室用高锰酸钾加热制取氧气时,选用的发生装置是
A
A
.(填编号,下同)用高锰酸钾制取氧气的文字表达式为
高锰酸钾
锰酸钾+二氧化锰+氧气
| 加热 |
高锰酸钾
锰酸钾+二氧化锰+氧气
;在加入药品前应对实验装置进行| 加热 |
检查装置的气密性
检查装置的气密性
检查.(3)若要收集一瓶较纯净的氧气应选择的收集装置是
E
E
,用该装置收集氧气完毕后的操作是先撤导管
撤导管
后熄灭酒精灯
熄灭酒精灯
,以防水倒吸炸裂试管;若收集到的氧气混有空气,可能原因是集气瓶中未装满水或刚开始产生气泡就立即收集
集气瓶中未装满水或刚开始产生气泡就立即收集
.(填一点即可)(4)二氧化碳是一种无色、能溶于水且密度比空气大的气体;可选用的收集装置是
C
C
.实验室用大理石(固体)和稀盐酸(液体)常温下反应来制取,生成水、二氧化碳和氯化钙,应选择的发生装置是B
B
;该反应的文字表达式碳酸钙+稀盐酸→二氧化碳+氯化钙+水
碳酸钙+稀盐酸→二氧化碳+氯化钙+水
.分析:(1)依据对常见仪器的认识及掌握解决此问题;
(2)根据实验室用加热高锰酸钾制取氧气的反应条件“固体加热”、操作注意事项进行解答;气体发生装置在加入药品前要检查装置的气密性;
(3)根据氧气的性质和对收集气体的要求,确定收集装置;用排水法收集氧气时,为了收集到较纯净的气体,必须将集气瓶装满水,并且要等导管口的气泡连续均匀冒出时再收集;
(4)根据二氧化碳是通过固体和液体在常温下反应制得,选择试验发生装置;再根据二氧化碳的密度大于空气的密度选择合适的收集装置.
(2)根据实验室用加热高锰酸钾制取氧气的反应条件“固体加热”、操作注意事项进行解答;气体发生装置在加入药品前要检查装置的气密性;
(3)根据氧气的性质和对收集气体的要求,确定收集装置;用排水法收集氧气时,为了收集到较纯净的气体,必须将集气瓶装满水,并且要等导管口的气泡连续均匀冒出时再收集;
(4)根据二氧化碳是通过固体和液体在常温下反应制得,选择试验发生装置;再根据二氧化碳的密度大于空气的密度选择合适的收集装置.
解答:解:(1)熟记常见仪器的名称和用途可知,仪器名称为:水槽、集气瓶;
(3)根据实验室用加热高锰酸钾制取氧气的反应条件“固体加热”所以选用的发生装置是A;高锰酸钾制取氧气可生成锰酸钾、二氧化锰和氧气,可写出反应的文字表达式;向气体发生装置内加入药品前,应该进行的操作是检查装置的气密性;
(3)氧气可用排水法和向上排空气法收集,但向上排空气法收集的气体可能混有空气,所以选E;实验完毕时,如果先灭灯,后撤导管,会使得水槽中的水倒流到热的试管中,使试管炸裂;用排水法收集到氧气时,为了收集到较纯净的气体,必须将集气瓶装满水,并且要等导管口的气泡连续均匀冒出时再收集;
(4)实验室制取二氧化碳的药品是大理石(固体)和稀盐酸(液体),且反应不需要加热,发生装置选用液固常温型发生装置,可用B;因为二氧化碳密度比空气的密度大,且能溶于水,所以用向上排空气法收集,收集装置可用C;
故答案为:
(2)A;高锰酸钾
锰酸钾+二氧化锰+氧气;检查装置的气密性;
(3)E;撤导管,熄灭酒精灯;集气瓶中未装满水,刚开始产生气泡就立即收集;
(4)C,B,碳酸钙+稀盐酸→二氧化碳+氯化钙+水.
(3)根据实验室用加热高锰酸钾制取氧气的反应条件“固体加热”所以选用的发生装置是A;高锰酸钾制取氧气可生成锰酸钾、二氧化锰和氧气,可写出反应的文字表达式;向气体发生装置内加入药品前,应该进行的操作是检查装置的气密性;
(3)氧气可用排水法和向上排空气法收集,但向上排空气法收集的气体可能混有空气,所以选E;实验完毕时,如果先灭灯,后撤导管,会使得水槽中的水倒流到热的试管中,使试管炸裂;用排水法收集到氧气时,为了收集到较纯净的气体,必须将集气瓶装满水,并且要等导管口的气泡连续均匀冒出时再收集;
(4)实验室制取二氧化碳的药品是大理石(固体)和稀盐酸(液体),且反应不需要加热,发生装置选用液固常温型发生装置,可用B;因为二氧化碳密度比空气的密度大,且能溶于水,所以用向上排空气法收集,收集装置可用C;
故答案为:
(2)A;高锰酸钾
| 加热 |
(3)E;撤导管,熄灭酒精灯;集气瓶中未装满水,刚开始产生气泡就立即收集;
(4)C,B,碳酸钙+稀盐酸→二氧化碳+氯化钙+水.
点评:可根据反应物的状态及其反应条件选择发生装置,反应物为固体需要加热,则选择固体加热型发生装置,反应物为固体和液体,在常温下就能反应,则选择液固常温型发生装置,根据气体的密度和水溶性选择收集装置,难溶于水的气体能使用排水法收集,密度比空气大的气体能使用向上排空气法收集,密度比空气小的气体能使用向下排空气法收集.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目

 化学实验是学习化学和进行科学研究的重要方法和途径.学会气体物质的制备方法是研究气体、利用气体的基础.请根据图回答有关问题:
化学实验是学习化学和进行科学研究的重要方法和途径.学会气体物质的制备方法是研究气体、利用气体的基础.请根据图回答有关问题: