题目内容
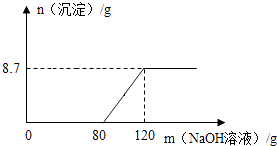
【题目】将5%的NaOH溶液逐滴加入到10克稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示. 试回答: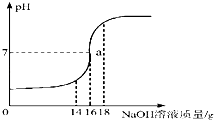
(1)a点溶液中大量存在的离子有 . (写符号)
(2)当恰好完全反应时,消耗NaOH溶液的质量为克.
(3)计算稀盐酸中溶质的质量分数: .
【答案】
(1)Na+、Cl﹣
(2)16
(3)7.3%
【解析】解:(1)a点时氢氧化钠与氯化氢恰好反应生成氯化钠,则该溶液中大量存在的离子为:Na+、Cl﹣ ,
所以答案是:Na+、Cl﹣;(2)根据图示可知,两溶液恰好完全反应时消耗NaOH溶液的质量为16g,
所以答案是:16;(3)设稀盐酸中氯化氢的质量为x,
NaOH+ | HCl═NaCl+H2O, |
40 | 36.5 |
16g×5% | X |
则: ![]() =
= ![]() ,
,
解得:x=0.73g,
稀盐酸中溶质的质量分数为: ![]() ×100%=7.3%,
×100%=7.3%,
所以答案是:7.3%.
【考点精析】通过灵活运用中和反应及其应用和质量守恒定律及其应用,掌握中和反应:酸与碱作用生成盐和水的反应;①质量守恒定律只适用于化学变化,不适用于物理变化;②不参加反应的物质质量及不是生成物的物质质量不能计入“总和”中;③要考虑空气中的物质是否参加反应或物质(如气体)有无遗漏即可以解答此题.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案
相关题目
【题目】氧气是一种化学性质较活泼的气体,能与许多物质反应。下列物质在足量氧气中燃烧的生成物中,错误的是( )
选项 | A | B | C | D |
物质 | 硫 | 铁 | 木炭 | 氢气 |
在氧气中燃烧的产物 | 二氧化硫 | 三氧化二铁 | 二氧化碳 | 水 |
A. A B. B C. C D. D