��Ŀ����
����Ŀ��A��I�dz��л�ѧ���������ʣ�����֮������ϵ��ͼ��ʾ����������ָ�������������B�Ǻ���ɫ��ĩ��A��C�����������壬H��I�к���һ����ͬԪ�أ�H������ϡ���ᣬI�Ǻ��ɫ���壮��ش��������⣺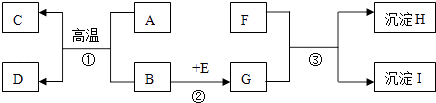
��1��д�����ʵĻ�ѧʽ��I�� �� H�� ��
��2����Ӧ�۵Ļ�����Ӧ������ ��
��3������F��������ᡱ����������Ρ������������
��4����Ӧ�ٵĻ�ѧ����ʽΪ����Ӧ�ڵĻ�ѧ����ʽΪ ��
���𰸡�
��1��Fe��OH��3��BaSO4
��2�����ֽⷴӦ
��3����
��4��3CO+Fe2O3 ![]() 2Fe+3CO2��Fe2O3+3H2SO4=Fe2��SO4��3+3H2O
2Fe+3CO2��Fe2O3+3H2SO4=Fe2��SO4��3+3H2O
���������⣺B�Ǻ�ɫ��ĩ��A��C�����������壬A��B���»�����C��D������A��һ����̼��B������������������һ����̼�����������Ͷ�����̼������C�Ƕ�����̼��D����������������F������������E���ɵ�G��F���������ֳ�����H��I�к���һ����ͬԪ�أ�H������ϡ���ᣬI�Ǻ��ɫ���壬����I�������������ɫ���壬H�����ᱵ������E�����ᣬG����������F������������������������������Ӧ���������������������ᱵ������������֤���Ƶ���ȷ����ˣ���1������������֪��I��������������ѧʽΪ��Fe��OH��3 �� H�����ᱵ����ѧʽΪ��BaSO4 ��
�ʴ�Ϊ��Fe��OH��3 �� BaSO4����2����Ӧ����������������������Ӧ���������������������ᱵ������3Ba��OH��2+Fe2��SO4��3=2Fe��OH��3��+3BaSO4������Ӧ�����ֻ�����������ɷ������������ֻ�����ķ�Ӧ����Ӧ����Ԫ�ػ��ϼ۱仯���ڸ��ֽⷴӦ��
�ʴ�Ϊ�����ֽⷴӦ����3������F����������������ˮ�������������ȫ�������������ӵĻ��������ڼ
�ʴ�Ϊ�����4����Ӧ����һ����̼���������ڸ��µ������·�Ӧ�������Ͷ�����̼����ѧ����ʽΪ��3CO+Fe2O3 ![]() 2Fe+3CO2 �� ��Ӧ���������������ᷴӦ������������ˮ����Ӧ�Ļ�ѧ����ʽΪ��Fe2O3+3H2SO4=Fe2��SO4��3+3H2O��
2Fe+3CO2 �� ��Ӧ���������������ᷴӦ������������ˮ����Ӧ�Ļ�ѧ����ʽΪ��Fe2O3+3H2SO4=Fe2��SO4��3+3H2O��
�ʴ�Ϊ��3CO+Fe2O3 ![]() 2Fe+3CO2��Fe2O3+3H2SO4=Fe2��SO4��3+3H2O��
2Fe+3CO2��Fe2O3+3H2SO4=Fe2��SO4��3+3H2O��
����A��I�dz��л�ѧ���������ʣ�B�Ǻ�ɫ��ĩ��A��C�����������壬A��B���»�����C��D������A��һ����̼��B������������������һ����̼�����������Ͷ�����̼������C�Ƕ�����̼��D��������������E���ɵ�G��F���������ֳ�����H��I�к���һ����ͬԪ�أ�H������ϡ���ᣬI�Ǻ��ɫ���壬����I�������������ɫ���壬H�����ᱵ������E�����ᣬG����������F������������������������������Ӧ���������������������ᱵ������Ȼ���Ƴ������ʽ�����֤���ɣ���1��������֪I������������H�����ᱵ����2����Ӧ����������������������Ӧ���������������������ᱵ��������3������F�������������ڼ��4����Ӧ����һ����̼���������ڸ��µ������·�Ӧ�������Ͷ�����̼����Ӧ���������������ᷴӦ������������ˮ��

����Ŀ��ij���������к���̼������ʣ���ȡ��ϸ�ĸ���Ʒ12.4g������ƿ�У�����32.6gˮ��������γ�����Һ��������ƿ����εμ�����ʹ���ַ�Ӧ�������ݲ�������ü����������������ƿ�����ʵ�������ϵ���±���ʾ��
�������������/g | 0 | 25 | 37.5 |
��ƿ�����ʵ�����/g | 45 | 70 | 80.3 |
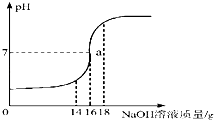
��1�����������������0��25gʱ�������ᷢ����Ӧ��
��2����Ӧ����������̼������Ϊg��
��3������Ʒ���������Ƶ�����������д��������̣���ȷ��0.1%����