题目内容
【题目】向盛有100g稀硫酸的烧杯中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入NaOH溶液,所得沉淀质量与加入NaOH溶液的质量关系如图所示,求 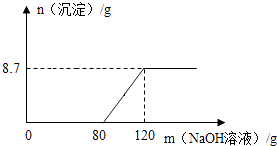
(1)镁粉的质量;
(2)NaOH溶液的溶质质量分数.
【答案】
(1)解:由图8可知,生成的Mg(OH)2质量为8.7g,则:
Mg(OH)2中金属镁的质量即为镁粉的质量:8.7g× ![]() =3.6g
=3.6g
(2)解:由图8可知,与硫酸镁反应的NaOH溶液质量为120g﹣80g=40g
设NaOH溶液的溶质质量分数为x,则
2NaOH+MgSO4═Na2SO4+ | Mg(OH)2↓ |
2×40 | 58 |
40g×x | 8.7g |
![]() =
= ![]()
x=30%
【解析】(1)根据Mg(OH)2中金属镁的质量即为镁粉的质量解答;(2)根据稀硫酸和镁反应生成硫酸镁和氢气,硫酸镁和氢氧化钠反应生成氢氧化镁沉淀和硫酸钠,根据反应的化学方程式和提供的数据可以进行相关方面的计算.
【考点精析】根据题目的已知条件,利用根据化学反应方程式的计算的相关知识可以得到问题的答案,需要掌握各物质间质量比=系数×相对分子质量之比.

练习册系列答案
相关题目