题目内容
【题目】同学们利用如图装置进行氧气实验与二氧化碳有关性质的探究。
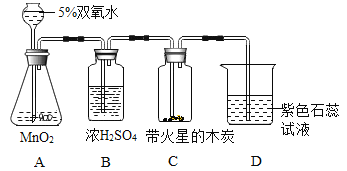
(1)写出装置A中发生反应的化学方程式:_____。
(2)装置C中的实验现象是:_____,说明氧气的化学性质_____。
(3)装置D中紫色石蕊试液变红色,说明溶液从中性变为_____,间接证明了_____。
【答案】2H2O2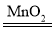 2H2O+O2↑ 木炭剧烈燃烧,发出白光 能支持燃烧 酸性 二氧化碳与水反应生成了酸
2H2O+O2↑ 木炭剧烈燃烧,发出白光 能支持燃烧 酸性 二氧化碳与水反应生成了酸
【解析】
(1)装置A中过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(2)生成氧气后,装置C中带火星的木炭在氧气中燃烧,会观察到剧烈燃烧,发出白光,木炭在氧气中燃烧更旺,说明氧气能支持燃烧;
(3)紫色石蕊溶液遇酸性溶液变红,遇碱性溶液变蓝,木炭在氧气中燃烧生成二氧化碳,装置D中紫色石蕊试液变红色,说明溶液从中性变为酸性,间接证明了二氧化碳与水反应生成了酸。

 阅读快车系列答案
阅读快车系列答案【题目】某化学小组在实验室用CO和Fe2O3在密闭容器中隔绝空气加强热模拟炼铁过程,一段时间后收集到如下数据:
物质 | CO | Fe2O3 | Fe | M | CO2 |
反应前质量(g) | 2.8 | 16 | 0 | 0 | 0 |
反应后质量(g) | 0 | 0 | 0 | a | b |
(1)预期看到的实验现象应该是_____________________________;
(2)表中b的值为____________;物质M的化学式为_______________。
【题目】化学课堂上,同学们在老师的指导下进行了分组实验。
(查阅资料)氯化钙溶液、氯化钠溶液都呈中性。
(1)第I组实验:探究酸和碱的反应。向试管中加入少量的氢氧化钙溶液,并滴入几滴无色酚酞溶液,充分振荡后,再逐滴滴入稀盐酸,并用玻璃棒不断搅拌,观察到溶液由红色变为无色,测得溶液的pH<7.该过程中发生反应的化学方程式为________,反应后溶液中的溶质为________。
(2)第Ⅱ组实验:为了探究一瓶忘记盖瓶塞的氢氧化钠溶液中溶质的成分,同学们进行了如下实验。
(提出猜想)
猜想1;溶质是氢氧化钠;
猜想2:溶质是________;
猜想3:溶质是碳酸钠。
(设计实验)
实验步骤 | 实验现象 | 实验结论 |
取少量样品于试管中,向其中加入适量的氯化钡溶液,充分反应后,过滤,向滤液中滴加几滴无色酚酞溶液 | ________ | 猜想3成立 发生反应的化学方程式为________。 |
(交流讨论)
老师问:“若向少量样品中,加入足量的稀盐酸,如果有气泡产生,猜想3一定成立吗?”同学们交流讨论后,一致认为猜想3不一定成立,原因是________。
(3)实验结束后,同学们将两组实验后的废液倒入同一个废液缸中进行集中处理。若使废液中只含有一种溶质氯化钠(酚酞除外)则需向废液中加入________。