题目内容
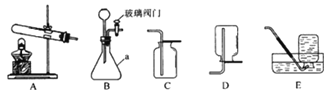
【题目】某实验小组在探究硫酸铜的化学性质时,做了如图所示的三组实验.

(1)实验一:探究硫酸铜溶液的酸碱性,用pH试纸测得pH<7,则说明硫酸铜溶液呈 性.
实验二:探究硫酸铜溶液与金属的反应.观察到试管A中有 现象时,说明铁与硫酸铜溶液发生了反应;而试管B中无明显现象,则铜、铁、银三种金属活动性由强到弱的顺序依次是 .
实验三:探究硫酸铜与碱溶液的反应.观察到试管C中产生蓝色沉淀,该反应的化学方程式为 .
(2)小组同学将实验三中所得混合物过滤,得蓝色固体和无色滤液.对滤液中溶质的成分展开探究.
【提出问题】滤液中溶质的成分是什么?
【猜想假设】滤液中溶质的成分有 种可能.
【实验验证】取少量滤液与试管中,向其中滴加几滴无色酚酞溶液,溶液变红,则滤液中的溶质是 .
【拓展迁移】小组同学欲将得到的蓝色固体转化成硫酸铜溶液,可向其中加入适量的 .
【答案】
(1)酸;铁表面会附着红色物质,溶液逐渐由蓝色变为浅绿色;铁>铜>银;2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;(2)两;Na2SO4和NaOH;稀硫酸
【解析】
试题分析:(1)实验一:用pH试纸测得pH<7,则说明硫酸铜溶液呈酸性;实验二:铁与硫酸铜反应生成硫酸亚铁和铜,铁表面会附着红色物质,溶液逐渐由蓝色变为浅绿色,因为生成的硫酸亚铁的溶液呈浅绿色所以随着反应的进行溶液逐渐变为浅绿色.证明铁的活动性大于铜,而试管B中无明显现象,证明银的活动性小于铜;所以三种金属活动性由强到弱的顺序依次是铁>铜>银;实验三:硫酸铜与氢氧化钠反应生成硫酸钠和氢氧化铜,方程式为:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4.(2)
【猜想假设】硫酸铜与氢氧化钠恰好反应,滤液中溶质为Na2SO4.如果硫酸铜过量,滤液中溶质为Na2SO4和CuSO4;如果氢氧化钠过量,滤液中溶质为Na2SO4和NaOH.又因为无色滤液,所以硫酸铜不可能过量.
【实验验证】向其中滴加几滴无色酚酞溶液,溶液变红,说明含有NaOH,所以滤液中溶质为Na2SO4和NaOH.
【拓展迁移】氢氧化铜与硫酸反应生成硫酸铜和水.故答案为:酸;铁表面会附着红色物质,溶液逐渐由蓝色变为浅绿色;铁>铜>银;2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;(2)两;Na2SO4和NaOH;稀硫酸