题目内容
【题目】以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究并帮忙填写空格(包括表中的空格)。
【提出问题】化学反应前后各物质的质量总和是否相等?
【猜想与假设】猜想1:不相等; 猜想2:相等。
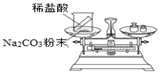
【实验探究】甲、乙两组同学用托盘天平分别称量反应前后物质的质量。
甲组 | 乙组 | |
实验方案(反应后略) |
|
|
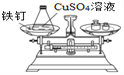
实验现象 | 有气泡产生,天平指针向右偏转 | 铁钉表面 ______,溶液____,天平指针_________偏转 |
结论 | 猜想1正确。有关反应的方程式是:Na2CO3+2HCl | 猜想2正确。反应的化学方程式:___________________ |
【反思评价】究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体溢出,导致指针向右偏转。得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡是有气体生成或参加的反应一定要在____________中进行。
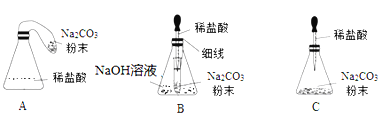
【优化装置】同学们对甲组左盘中的反应装置进行了如下三种改进,你认为最佳装置是___(填序号),从另外两种装置中任选一种指出其不足______(已知NaOH溶液能完全吸收CO2气体)
【得出结论】同学们利用改进后的最佳装置进行再次探究,均得出猜想二正确。进一步分析发现,反应体系中器材和未参加反应的物质的质量在反应前后保持不变,最终得出结论是:____的各物质的质量总和等于反应后生成的各物质的质量总和。
【解释应用】解释:化学反应前后,原子的种类、数目、质量均不变,所以质量守恒。
应用:某固体物质受热会发生分解反应,生成氧化铜、水和二氧化碳三种物质,则该固体物质一定由_________种元素组成。
【答案】 有红色固体 由蓝色变成浅绿色 没有或不发生 Fe+CuSO4![]() Cu+ FeSO4 密闭容器 B C中可能气压过大导致塞子冲出或A中气球中充满气体产生浮力影响实验 参加反应 4
Cu+ FeSO4 密闭容器 B C中可能气压过大导致塞子冲出或A中气球中充满气体产生浮力影响实验 参加反应 4
【解析】【实验探究】乙组:铁与硫酸铜反应,生成硫酸亚铁和铜,故铁钉表面有红色物质析出,溶液由蓝色变成浅绿色,天平指针没有偏转;反应的化学方程式:Fe+CuSO4=Cu+ FeSO4;【反思评价】通过讨论,同学们发现甲组中有气体溢出,导致指针向右偏转.得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在密闭中进行;【优化装置】最佳装置是B,A同学实验中碳酸钠与盐酸反应生成二氧化碳,二氧化碳充满气球,使整个装置所受空气浮力增大,因此反应后天平不能平衡;C中碳酸钠粉末与盐酸反应太快,橡皮塞易弹出;【得出结论】参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和;【解释应用】因为化学反应前后元素的种类不变,氧化铜、二氧化碳和水含有铜、碳、氧、氢四种元素,所以该化合物中也会含有这四种元素。

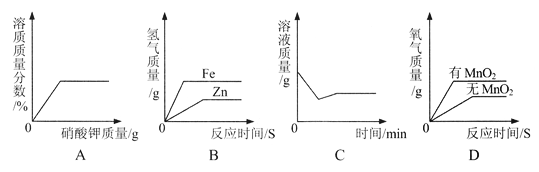
【题目】为了测定混有少量杂质的高锰酸钾固体样品中高锰酸钾的质量分数,取20g样品加热(杂质不反应),剩余固体的质量与加热时间的关系如表所示:
加热时间/min | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
剩余固体质量/g | 20 | 20 | 19.6 | 18.8 | 18.6 | 18.4 | 18.4 |
(1)t0至t1时间段,固体质量不变的原因是____________________________。
(2)反应中产生氧气的质量是_________。
(3)求样品中高锰酸钾的质量分数_________。
(4)该反应中转化为氧气的氧元素质量占高锰酸钾中氧元素质量的________%。
【题目】某校兴趣小组在实验室中完成制取氧气的实验。他们取氯酸钾和二氧化锰的混合物共5.0 g放入大试管中加热,并在不同时刻测定试管内剩余固体物质的质量(如下表):
反应时间/min | 1.0 | 2.0 | 3.0 | 4.0 | 5.0 |
剩余固体质量/g | 4.55 | 3.75 | 3.30 | 3.08 | 3.08 |
分析表中数据,完成下列问题:
(1)完全反应后,生成氧气的质量为________g;
(2)原混合物中氯酸钾的质量分数是多少?(精确到0.1%)
【题目】空气中氧气含量测定的再认识。
[经典赏析] 资料:金属汞和氧气加热生成氧化汞,氧化汞高温分解又生成氧气和金属汞。
法国化学家拉瓦锡用定量的方法研究了空气的成分(实验装置如图所示)。该实验中选择使用汞的优点有________。

A.实验过程中没有污染
B.在汞槽中起到液封的作用
C.生成的氧化汞加热分解又能得到汞和氧气
D.能将密闭装置内空气中的氧气几乎耗尽
[实验回顾] 如下图是实验室用红磷燃烧来粗略测定空气中氧气含量的装置。

(1)写出红磷燃烧的文字表达式:__________________________________。
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内________减小,烧杯中的水倒吸到集气瓶。若装置的气密性良好,操作规范,用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量。
[问题提出] 有实验资料表明:燃烧过程中当氧气体积分数低于7%时,红磷就无法继续燃烧,因此通过上述实验,测量结果与理论值误差较大。
[实验改进]
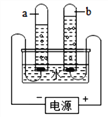
Ⅰ.根据铁在空气中生锈的原理设计如下图所示实验装置,再次测定空气中氧气的含量。装置中饱和食盐水、活性炭会加速铁生锈。

Ⅱ.测得实验数据如下表:
测量 项目 | 实验前 | 实验后 | |
烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
体积/mL | 80.0 | 54.5 | 126.0 |
[交流表达]
(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁。写出该反应的文字表达式:______________________________________________。
(2)根据表格数据计算,改进实验后测得的空气中氧气的体积分数是________(计算结果精确到0.1%)。
(3)从实验原理角度分析,改进后的实验结果比前者准确度更高的原因是:
①________________________________________________________________________;
②________________________________________________________________________。
【题目】课本“分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性质实验,引起了化学探究小组的兴趣。
【提出问题】氧化铁(Fe2O3)能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
【实验探究】
实验步骤 | 实验现象 |
Ⅰ.分别量取5mL5%过氧化氢溶液放入A、B两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象。 | A试管中产生气泡,带火星木条复燃, B试管中无明显现象 |
Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 | 试管中均产生气泡,带火星木条均复燃 |
Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag. | |
Ⅳ.分别量取5mL5%过氧化氢溶液放入C、D两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象。 |
【实验结论】
(1)实验Ⅱ、Ⅲ证明:氧化铁的______和____________在反应前后均没有发生变化,可以作过氧化氢溶液分解的催化剂。
(2)写出氧化铁(Fe2O3)催化过氧化氢溶液分解的符号表达式_____________________。
【试验评价】实验设计Ⅳ的目的是比较_____________________。
【实验拓展】查阅资料得知:硫酸铜、马铃薯等也可以作过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是______________(填序号)。
A.MnO2是所有反应的催化剂
B.同一个化学反应可以有多种催化剂
C.催化剂只能加快化学反应速率
D.用作催化剂的物质也可能是其他反应的反应物或生成物