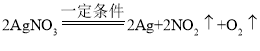题目内容
【题目】湿地之都,水绿盐城!
(1)新四军纪念馆是盐城市的名片之一。馆内有许多抗战时的枪炮,但有些表面出现锈迹,其主要原因是:铁与_______等物质共同作用的结果。稀盐酸可用来除铁锈,化学方程式为_______。
(2)郭猛的温泉度假村是人们休闲的好去处。
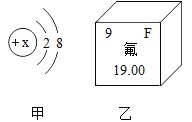
①温泉水富含钾、钙、镁、氟、硅等,这里的“钾、钙、镁、氟、硅”指的是_______(填序号)。
A 分子 B 原子 C 元素 D 单质
②温泉水的pH在7.5~8.9之间,若先将pH试纸用蒸馏水润湿,再进行测定,则所测得的结果_______(填“偏大”、“偏小”或“不受影响”)。
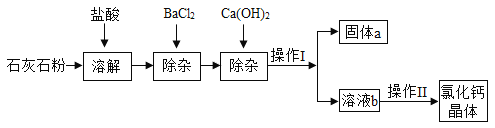
(3)自来水的生产过程如图所示。
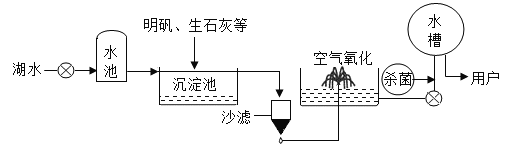
①上述生产过程中使用的净水方法有_______(填序号)。
A 沉淀 B 过滤 C 煮沸 D 蒸馏
②自来水用氯气杀菌消毒。请将下列化学方程式补充完整:Cl2+ H2O = HClO +_______。
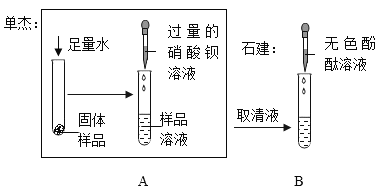
③能否用硝酸银区分该厂的自来水和蒸馏水________(填“能”或“不能”)。
(4)清洗餐具上的油污,常在水中加少量洗洁精,洗洁精所起的作用是_______。
(5)配制10%的氯化钠溶液时,会引起溶液中氯化钠质量分数偏大的是_______(填序号)。
A 用量筒量取水时俯视读数 B 配制溶液的烧杯中残留少量蒸馏水
C 氯化钠晶体不纯 D 转移已配好的溶液时,有少量溶液溅出
【答案】O2 、H2O Fe2O3 +6HCl=2FeCl3+3H2O C 偏小 A B HCl 能 乳化作用 A
【解析】
(1)铁生锈是铁与空气中的氧气和水共同作用的结果,故填O2、H2O;
铁锈的主要成分是氧化铁,盐酸能与氧化铁反应生成氯化铁和水,所以可用稀盐酸来除铁锈,故反应的化学方程式写为:Fe2O3+6HCl=2FeCl3+3H2O。
(2)①温泉水富含钾、钙、镁、氟、硅等,这里的“钾、钙、镁、氟、硅”指的是物质的组成,指的是元素,故填C;
②温泉水的pH在7.5~8.9之间,所以温泉水呈碱性,若先将pH试纸用蒸馏水润湿,则被测的温泉水的碱性被稀释而减弱,测得的pH偏小,故填偏小。
(3)①自来水厂生产自来水的步骤有沉降、过滤、吸附、杀菌等,不需要煮沸和蒸馏,故填AB;
②由化学方程式可知,反应前出现了2个氯原子、2个氢原子和1个氧原子,反应后出现了1个氢原子、1个氯原子和1个氧原子,根据质量守恒定律可知,反应后尚缺少1个氢原子和1个氯原子,所以空格处物质的化学式为HCl,故填HCl;
③自来水中含有的可溶性杂质中含有氯化镁、氯化钙等物质,其中的氯离子可与硝酸银中的银离子结合生成氯化银白色沉淀,蒸馏水中不含氯离子,加入硝酸银溶液后不会产生白色沉淀,所以能用硝酸银溶液区分自来水和蒸馏水,故填能。
(4)洗洁精具有乳化作用,能够乳化油污,可用洗洁精来清洗餐具上的油污,故填乳化作用。
(5)A 用量筒量取水时俯视读数,读数大于液体的实际体积数,则量取的水的体积较小,配制的溶液的溶质质量发生偏大,选项正确;
B 配制溶液的烧杯中残留少量蒸馏水,配制的溶液中溶剂水的质量偏多,所配溶液的溶质质量分数偏小,选项错误;
C 氯化钠晶体不纯,则配制的溶液中的溶质的质量偏少,所配溶液的溶质质量分数就会偏小,选项错误;
D 转移已配好的溶液时,有少量溶液溅出只减少了溶液的质量,不改变溶液的溶质质量分数,选项错误。故填A。