题目内容
【题目】酸、碱和盐是初中化学学习和研究的重要内容。
(1)熟石灰在生产和生活中有广泛的用途,下列不属于熟石灰的用途的是____________(填字母)。
A改良酸性土壤
B工厂处理含有硫酸的废水
C农业上配制波尔多液
D用作干燥剂
(2)酸能与活泼金属发生反应。若将含有铁粉5.6 g、铜粉3.2 g的混合物与一定质量的稀硫酸充分反应,反应停止后,有6g固体剩余。则生成氢气的质量为______________g。
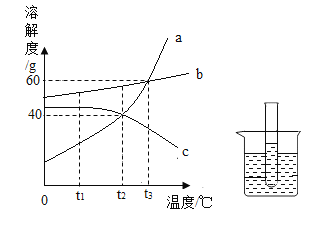
(3)酸和碱在化学实验探究中具有重要的应用。草酸分解会得到水蒸气与另外两种气体物质,某研究小组欲检验草酸( H2C2O4 )样品的分解产物,按下图所示装置进行实验。
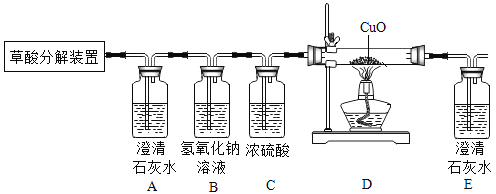
①该实验结束后为防止E处的溶液倒吸,正确的实验操作为____________________。
②实验中观察到A 、E中澄清石灰水变浑浊,D中固体由黑色变为紫红色,则说明草酸分解的另外两种物质是____________________;小花认为如果能够进一步验证B中仍有氢氧化钠剩余.则实验结论会更加准确。请设计实验证明B中仍含有氢氧化钠__________。
③该实验方案仍然有不足之处,请给出改进的实验方案:____________________。
(4)现有某石灰石样品16 g,向其中加入104. 4 g的稀盐酸,恰好完全反应后(杂质不溶解也不参加反应) ,称量得到剩余固液混合物总质量为116 g,请计算样品中碳酸钙的质量分数______________。
【答案】D 0.1 先断开装置DE的连接,然后熄灭酒精灯 二氧化碳和一氧化碳 取少量实验后B装置中的溶液置于试管中,向溶液中加入足量的氯化钙溶液,静置,再向上层清液中滴加无色酚酞溶液,若溶液变红,说明B中仍含氢氧化钠 在装置E的右端管口处放一只燃着的酒精灯,燃烧处理尾气 62.5%
【解析】
(1)A 属于碱的熟石灰能与酸发生中和反应,所以熟石灰可用于改良酸性土壤,选项正确;
B 属于碱的熟石灰能与酸发生中和反应,所以工厂处理含有硫酸的废水可用熟石灰,选项正确;
C 熟石灰能与硫酸铜溶液反应,可用于农业上配制波尔多液,选项正确;
D 熟石灰既不具有吸水性,也不能与水发生反应,所以熟石灰不能用作干燥剂,选项错误,故填D。
(2)铜不能与酸反应生成氢气,所以反应后剩余的6g固体的质量是铜和剩余的铁的质量和,则参加反应的铁的质量=5.6g(6g3.2g)=2.8g,由铁与硫酸反应的化学方程式Fe+H2SO4=FeSO4+H2↑可知,参加反应的铁与生成的氢气的质量比为56:2,则生成氢气的质量为2.8g×![]() =0.1g,故填0.1。
=0.1g,故填0.1。
(3)①实验结束后为防止E处的溶液倒吸,可以先断开装置DE的连接,然后熄灭酒精灯,故填先断开装置DE的连接,然后熄灭酒精灯;
②二氧化碳能与澄清的石灰水反应生成碳酸钙沉淀,从而使澄清石灰水变浑浊,A中澄清石灰水变浑浊,说明草酸分解的生成物中有二氧化碳,E中澄清石灰水变浑浊,D中固体由黑色变为紫红色,说明该反应是一氧化碳与氧化铜反应生成了红色固体铜和二氧化碳,从而说明草酸分解的生成物中还有一氧化碳,即草酸分解的生成物中除水蒸气外,还有二氧化碳和一氧化碳,故填二氧化碳和一氧化碳;
氢氧化钠与二氧化碳反应生成碳酸钠,碳酸钠与氢氧化钠溶液均呈碱性,而氯化钙能与碳酸钠反应生成碳酸钙沉淀和溶液呈中性的氯化钠,所以证明B中仍含有氢氧化钠的方法是取少量实验后B装置中的溶液置于试管中,向溶液中加入足量的氯化钙溶液,静置,再向上层清液中滴加无色酚酞溶液,若溶液变红,说明B中仍含氢氧化钠,故填取少量实验后B装置中的溶液置于试管中,向溶液中加入足量的氯化钙溶液,静置,再向上层清液中滴加无色酚酞溶液,若溶液变红,说明B中仍含氢氧化钠;
③该实验中缺少尾气处理装置,会造成尾气中的一氧化碳进入空气,进而污染空气,所以可以在装置E的右端管口处放一只燃着的酒精灯,燃烧处理尾气,故填在装置E的右端管口处放一只燃着的酒精灯,燃烧处理尾气。
(4)解:根据质量守恒定律,生成的二氧化碳的质量=16g+104.4g116g=4.4g
设样品中碳酸钙的质量为x
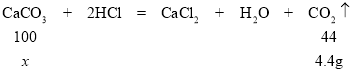
100:44=x:4.4g
x=10g
样品中碳酸钙的质量分数=![]() ×100%=62.5%
×100%=62.5%
答:样品中碳酸钙的质量分数是62.5%。

 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案