题目内容
【题目】根据下表回答问题。
温度/℃ | 20 | 40 | 50 | 60 | 80 | |
溶解度/g | NaCl | 36.0 | 36.6 | 37.0 | 37.3 | 38.4 |
NH4Cl | 37.2 | 45.8 | 50.4 | 55.2 | 65.6 | |
KNO3 | 31.6 | 63.9 | 85.5 | 110 | 169 | |
(1)20℃时,溶解度最大的物质是__________
(2)50℃时,在100g水中放入36g氯化钠充分溶解持温度降到40℃,得到的是氯化钠的溶液__________(选填“饱和”或“不饱和”):
(3)现将100gKNO3和38gNaCl同时放入一个盛有100克80℃水的烧杯中,然后降温至20℃,得到的溶液中,KNO3的溶质质量分数的计算式为__________。
【答案】![]() 不饱和
不饱和 ![]()
【解析】
(1)从表格中数据可以看出,20℃时,NH4Cl的溶解度最大;
(2)从表格中数据可知,50℃时氯化钠的溶解度是37.0g,将36g氯化钠充分溶解在100g水中,全部溶解,形成不饱和溶液,降温至40℃,40℃氯化钠的溶解度是36.6g,溶液仍是不饱和溶液;
(3)80℃时KNO3溶解度是169g,80℃时NaCl的溶解度是38.4g,将100gKNO3和38gNaCl同时放入一个盛有100g80℃水的烧杯中,能全部溶解,然后降温至20℃,20℃KNO3溶解度31.6g,KNO3要析出68.4g ,20℃NaCl的溶解度是36.0g,NaCl要析出2.4g,此时形成的溶液共100g+31.6g+36.0g,KNO3溶质质量分数计算式为:![]() 。
。

【题目】如图的加热袋常用于野外加热食物。加热袋中的固体粉末含镁粉、铁粉和氯化钠,使用时向其中加入水袋中的水,即可产生大量热。实验小组针对放热过程中的反应原理展开探究。


【查阅资料】
常温下镁粉能与水发生置换反应,且放热。
【进行实验】
同学们用下图所示装置进行模拟实验:分别取不同成分的固体粉末放入甲中,通过分液漏斗向其中均加入8 mL水,读取甲中所得固液混合物的最高温度,实验记录如下表:
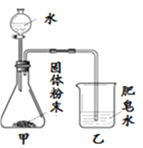
(实验时的室温为22.8℃)
实验序号 | A | B | C | D | E | F |
固体成分 | Mg | Fe | Mg+Fe | Mg+NaCl | Fe+NaCl | Mg+Fe+NaCl |
乙中现象 | 少量肥皂泡,难以点燃 | ______ | 少量肥皂泡,难以点燃 | 较多肥皂泡,点燃有爆鸣声 | 无肥皂泡 | 大量肥皂泡,点燃有爆鸣声 |
混合物温度 | 23.1℃ | 22.8℃ | 23.1℃ | 24.2℃ | 22.8℃ | 27.2℃ |
【解释与结论】
(1)实验B,乙中现象为_______________。
(2)实验A证明了镁粉与水能反应,完成该反应的化学方程式Mg+2H2O=____+H2 ![]() 。
。
(3)使镁粉与水迅速反应并放热的最佳方法是向镁粉中加入_____________。
【反思改进】
(4)同学们分析实验数据发现,升高的温度没有达到食品加热袋的效果,其可能的原因是___________。
(5)同学们根据实验结果进一步猜测,实验F中的反应结束后,甲中剩余固体混合物中仍然含有铁粉,检验其铁粉存在的的验方案为:取少量固体混合物________。
(6)从上述实验初步得出“NaCl溶于水没有热量的变化”的结论,依据的两个实验是(填实验序号)______________。