��Ŀ����
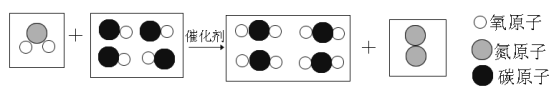
����Ŀ��ͼ�� A��F �Ǿ��꼶��ѧǰ�ĵ�Ԫ�еij������ʣ����� A��B ���ֻ�������ɵ�Ԫ����ͬ��B ��һ����������������������ʣ�C��D��E ��Ϊ���ʣ��� E �� C ��Ӧʱ������Ϊ����ȼ�գ��������䣬���ȣ��к�ɫ�������ɣ�ͼ����������ʾ���˵����ʼ��ܷ�����ѧ��Ӧ����������ʾ���ʼ����ת����ϵ����Ӧ���������ַ�Ӧ�������������ȥ��
��1��д���������ʵ�����
A_______ C_______ F_______ ��
��2��д�����з�Ӧ�Ļ�ѧ����ʽ��������Ӧ����
��B ���� C �� D_______,_______ ��������Ӧ���ͣ���
��C �� E ��Ӧ_______,_______��������Ӧ���ͣ���
���𰸡��������� ���� ���������� 2H2O![]() 2H2��+O2�� �ֽⷴӦ 3Fe+2O2
2H2��+O2�� �ֽⷴӦ 3Fe+2O2![]() Fe3O4 ���Ϸ�Ӧ
Fe3O4 ���Ϸ�Ӧ
��������
����Ŀ������������A��B ���ֻ�������ɵ�Ԫ����ͬ��B��һ����������������������ôBΪˮ��AΪ�������⣻B�������ɵ���C��D���ҵ���E �� C ��Ӧʱ������Ϊ����ȼ�գ��������䣬���ȣ��к�ɫ�������ɣ�������֪CΪ������EΪ������ôDΪ������E��F�����ת����F������Ԫ�أ���C������F����ôF��������������
��1���ɷ�����֪�����ʵ����ƣ�A���������⣻C��������F��������������
��2����B ���� C �� D��ˮ��ͨ���������������������������ѧ����ʽΪ2H2O![]() 2H2��+O2�����÷�Ӧ��һ�����ʷֽ������������ʣ����ڷֽⷴӦ��
2H2��+O2�����÷�Ӧ��һ�����ʷֽ������������ʣ����ڷֽⷴӦ��
��C �� E ��Ӧ����˿��������ȼ��������������������ѧ����ʽΪ3Fe+2O2![]() Fe3O4���÷�Ӧ����������������һ�����ʣ����ڻ��Ϸ�Ӧ��
Fe3O4���÷�Ӧ����������������һ�����ʣ����ڻ��Ϸ�Ӧ��

 �Ͻ�ƽСѧ��������ϵ�д�
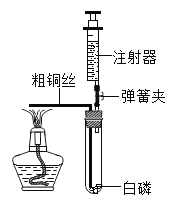
�Ͻ�ƽСѧ��������ϵ�д�����Ŀ��Ϊ̽����ѧ��Ӧǰ�����ʵ�������ϵ���������ʵ�鷽����
ʵ��ԭ������������ͭ��Һ��Ӧ��
ʵ����Ʒ���ٴ�������ά��ƿ����������ƽ��
ʵ��ҩƷ���ٴ�ĥ�õ���������װ���Լ�ƿ���������������Һ��
�����������¼������ʵ�����m1
�����ȱ����������ͭ��Һ�У����������������¼������ʵ�����m2
��1��д������������ͭ��Һ��Ӧ�Ļ�ѧ����ʽ��______________
��2��������У���αȽϺ����س�����������ʵ�����m1��_______________________
��3��ʵ�����������¼��������ݡ�������ɿհ״�����д
��������Ʒ | ���� | |
������������������m1 | ����������ƿ | ˮ��_______ |
������������������m2 | ����������ƿ | ˮ��_______ |
ʵ����� | _______ | |
����Ŀ�������±��ش����⡣
�¶�/�� | 20 | 40 | 50 | 60 | 80 | |
�ܽ��/g | NaCl | 36.0 | 36.6 | 37.0 | 37.3 | 38.4 |
NH4Cl | 37.2 | 45.8 | 50.4 | 55.2 | 65.6 | |
KNO3 | 31.6 | 63.9 | 85.5 | 110 | 169 | |
��1��20��ʱ���ܽ������������__________
��2��50��ʱ����100gˮ�з���36g�Ȼ��Ƴ���ܽ���¶Ƚ���40�棬�õ������Ȼ��Ƶ���Һ__________��ѡ��������������������������
��3���ֽ�100gKNO3��38gNaClͬʱ����һ��ʢ��100��80��ˮ���ձ��У�Ȼ������20�棬�õ�����Һ�У�KNO3���������������ļ���ʽΪ__________��