题目内容
【题目】金属在生活、生产中有着非常广泛的应用。请回答下列问题:
(1)2017年8月21日,“复兴号”中国标准动车组开跑京津城际,车体是铝合金制成,铝合金是_____ (填字母编号)。
A.有机合成材料 B.金属材料 C.复合材料
(2)十八世纪,化学家们研究发现某些金属与某些物质反应能生成一种气体,该气体被喻为“会制造水的物质”,对上述反应原理的认识加快了推翻燃素学说的进程。该气体在空气中燃烧制造水的化学方程式是_____。
(3)金属R不在初中学到的金属活动性顺序表中,已知R的活动性位于铜、铝之间,某同学为了验证这三种金属的活动性顺序,他选择了打磨过的金属R,你认为他还需要选择的另外两种溶液是_____溶液和________溶液。
(4)工业上常用铝土矿炼制铝,其主要成分为氧化铝,现用200t含氧化铝51%的铝土矿(其他成分不含铝)炼铝,假设在炼制过程中铝元素共计损失了10%,则反应后可制得铝_____t。
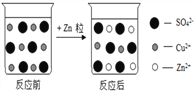
(5)铜与另一种金属M的混合物(M可能是铝、铁或银),在该混合物中加入足量的稀硫酸有气泡产生,待反应完成后过滤,得到铜和滤液,在滤液中加入锌片,其表面有一层黑色物质,则M是_____;取一定量的原混合物投入到一定量的硝酸银溶液中,充分反应后,对反应所得溶液和固体推断正确的是_____ (填字母编号)。
A.所得溶液中一定有M的离子 B.固体中一定有银和铜
C.固体中一定有银 D.所得溶液中一定有硝酸银
【答案】 (1)B; (2)2H2+O2![]() 2H2O; (3)硫酸铜; (4)硫酸铝; (5)48.6; (6)铁; (7)AC;
2H2O; (3)硫酸铜; (4)硫酸铝; (5)48.6; (6)铁; (7)AC;
【解析】(1)铝合金属于金属材料;(2)十八世纪,化学家们研究发现某些金属与某些物质反应能生成一种气体,该气体被喻为“会制造水的物质”,这种物质应该是氢气,氢气燃烧生成水,反应的化学方程式为:2H2+O2![]() 2H2O;(3)为了验证这三种金属的活动性顺序,他选择了打磨过的金属R,还需要选择的另外两种溶液是硫酸铜溶液和硫酸铝溶液,把R丝分别插入硫酸铜溶液、硫酸铝溶液中时,插入硫酸铜溶液中的R丝表面附着红色固体,说明R比铜活泼,插入硫酸铝溶液中的R丝表面无明显现象,说明铝比R活泼;(4)反应后可制得铝的质量为:200t×51%×
2H2O;(3)为了验证这三种金属的活动性顺序,他选择了打磨过的金属R,还需要选择的另外两种溶液是硫酸铜溶液和硫酸铝溶液,把R丝分别插入硫酸铜溶液、硫酸铝溶液中时,插入硫酸铜溶液中的R丝表面附着红色固体,说明R比铜活泼,插入硫酸铝溶液中的R丝表面无明显现象,说明铝比R活泼;(4)反应后可制得铝的质量为:200t×51%×![]() ×(1-10%)=48.6t;(5)在该混合物中加入足量的稀硫酸有气泡产生,说明M不是银,在滤液中加入锌片,其表面有一层黑色物质,说明锌表面附着的是铁,因此M是铁;A、M是铁,铁比铜活泼,取一定量的原混合物投入到一定量的硝酸银溶液中时,铁先和硝酸银反应,因此所得溶液中一定有亚铁离子,该选项说法正确;B、固体中一定有铁和硝酸银反应生成的银,不一定含有铜,这是因为如果硝酸银不足以和铁反应时,铜不能反应,该选项说法不正确;C、固体中一定有铁和硝酸银反应生成的银,该选项说法正确;D、所得溶液中不一定有硝酸银,这是因为如果硝酸银不足以和铁、铜反应时,溶液中不含有硝酸银,该选项说法不正确。
×(1-10%)=48.6t;(5)在该混合物中加入足量的稀硫酸有气泡产生,说明M不是银,在滤液中加入锌片,其表面有一层黑色物质,说明锌表面附着的是铁,因此M是铁;A、M是铁,铁比铜活泼,取一定量的原混合物投入到一定量的硝酸银溶液中时,铁先和硝酸银反应,因此所得溶液中一定有亚铁离子,该选项说法正确;B、固体中一定有铁和硝酸银反应生成的银,不一定含有铜,这是因为如果硝酸银不足以和铁反应时,铜不能反应,该选项说法不正确;C、固体中一定有铁和硝酸银反应生成的银,该选项说法正确;D、所得溶液中不一定有硝酸银,这是因为如果硝酸银不足以和铁、铜反应时,溶液中不含有硝酸银,该选项说法不正确。

【题目】实验加试中同学发现:向澄清石灰水中吹入![]() ,产生白色沉淀,再不断吹入
,产生白色沉淀,再不断吹入![]() ,沉淀全部溶解。同学们对白色沉淀溶解的生成物展开如下探究:
,沉淀全部溶解。同学们对白色沉淀溶解的生成物展开如下探究:
活动一:探究白色沉淀溶解的生成物是什么?
【查阅资料】碳酸钙、水和二氧化碳反应可生成碳酸氢钙。请完成资料里所涉及的化学方程式______。
活动二:探究碳酸氢钙具有哪些化学性质?
请你就碳酸氢钙可能具有的化学性质提出两个猜想并设计实验加以验证。可供使用的试剂和仪器为:![]() 溶液、
溶液、![]() 溶液、澄清石灰水、稀盐酸、NaOH溶液、试管、烧杯、导管、玻璃棒。
溶液、澄清石灰水、稀盐酸、NaOH溶液、试管、烧杯、导管、玻璃棒。
序号 | 猜想 | 操作步骤 | 可能观察到的现象 |
一 | ___________ | ___________ | ___________ |
二 | ___________ | ___________ | ___________ |
【题目】工业铁红主要成分是Fe2O3,还含有少量的FeO、Fe3O4
【查阅资料】(1)草酸晶体(H2C2O43H2O)在浓硫酸作用下受热分解,化学方程式为:H2C2O43H2O ![]() CO2↑+CO↑+H2O
CO2↑+CO↑+H2O
(2)碱石灰是固体NaOH和CaO的混合物,能吸收水蒸气和二氧化碳。
(3)铁的常见氧化物中铁的质量分数:
铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
铁的质量分数 | 77.8% | 70.0% | 72.4% |
【问题讨论】为了测定铁红中铁的质量分数,小组间进行如下实验。(装置气密性良好)
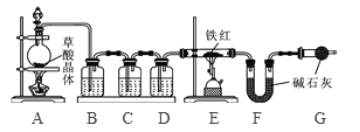
(1)该实验为了保证进入E中的气体是纯净、干燥的CO,则B、C、D中的试剂依次是________(填字母序号)
a.浓硫酸 b.澄清的石灰水 c氢氧化钠溶液
(2)C装置的作用是 __________________________。
(3)写出E装置中所发生反应的一个化学方程式: _____________________。
(4)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数。
①若E中充分反应后得到铁粉的质量为mg,则 ____ < m < ______。
②若实验前后称得F装置増重7.7g,则此铁红中铁的质量分数是 _________。
【实验反思】 (1)如果缺少G装置(不考虑其他因素),则测得样品中铁的质量分数会 ________(选填“偏小”“不变”“偏大”)。
(2)该实验装置的一个明显缺陷是 ___________________。