题目内容
【题目】现有25 g石灰石样品,请按下面要求计算:
(1)25 g样品与足量的稀盐酸反应放出8.8 gCO2(杂质不溶于酸,且不与酸反应),请计算该样品的纯度(CaCO3的质量分数)是多少________?
(2)若将一定质量的该石灰石样品高温煅烧,有关物质质量随反应时间的变化如表所示:
时间/min | t1 | t2 | t3 | t4 | t5 |
CO2质量/g | 2.2 | 4.4 | 6.6 | 8.8 | 8.8 |
剩余固体质量/g | 22.8 | 20.6 | m | 16.2 | 16.2 |
则m=_____,t3时剩余固体中除杂质外含有的物质是____(填化学式)。
【答案】80% 18.4; CaCO3和CaO
【解析】
(1)设该样品的纯度(CaCO3的质量分数)为x

![]() x=80%;
x=80%;
(2)根据质量守恒定律可得,m+6.6g=2.2 g+22.8 g,m=18.4 g;t4时、t5时固体质量不再减少,且为16.2 g,t3时固体为18.4 g,说明此时尚有碳酸钙没有完全分解,所以t3时剩余固体中除杂质外含有的物质是碳酸钙和氧化钙,对应的化学式为:CaCO3和CaO。

【题目】学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:氧化铜[CuO]能否起到类似MnO2的催化剂作用呢?于是进行了以下探究。
(猜想)
Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质都不变;
Ⅱ、CuO参与反应产生O2,反应前后质量和化学性质都发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后_____。
(实验)用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:
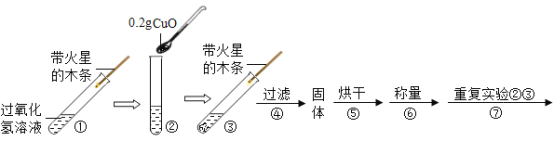
(1)填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
_____,带火星的木条复燃。 | _____ | 溶液中有气泡放出,_____ | 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立。 |
(2)过氧化氢能被CuO催化分解放出O2的反应式为_____。
(实验拓展):
(3)某同学想比较二氧化锰和氧化铜对过氧化氢分解的催化效果,他需要对某些变量进行控制,其中包括有:_____。(至少三点)
【题目】生活中我们经常发现存放的铁钉会生锈。

(1)小牛和小明通过如图所示实验对铁制品生锈的条件进行探究。通过观察和试管B中加入植物油的目的是___________________。我得出铁生锈的条件是_______________。
(2)在实验室用稀盐酸除铁锈的实验中,小牛认为盐酸中含有H2O、H+、Cl―三种粒子,为了探究稀盐酸中哪种粒子能使铁锈溶解,他进行了如下实验,我能帮他完成。
实验步骤 | 实验现象 | 实验结论 | 设计实验的目的 |
向装有锈铁钉的试管中加入足量NaCl溶液,振荡 | 铁锈不溶解 | _________ | _________ |
小明认为还需要补做一个“向装有锈铁钉的试管中加入水”的对比实验,我认为这个实验是多余的,理由是_____________。小明在做铁钉除锈实验时,由于忘了及时从稀盐酸中取出已除掉铁锈的铁钉,过了一段时间后,他发现铁钉表面居然出现了黑色物质。通过分析我认为铁钉表面的黑色物质可能是_____________。
(3)为了探究铁锈除掉后溶液的组成,小牛将生锈的铁钉放入一支试管中,加入一定量的稀盐酸,待铁钉表面的铁锈恰好溶解完时,迅速取出铁钉,再进行以下实验。
实验步骤 | 实验现象 | 实验结论 |
向取出铁钉的溶液中加入过量的铁粉 | _________ | _________ |
我能写出(3)中的一个化学方程式_________
(4)通过以上探究,我获得的启示是_____________。
【题目】某化学兴趣小组的同学对碳酸钙高温加热一段时间剩余固体的成分进行探究。
(提出问题)加热后剩余固体的成分是什么?
(猜想与探究)
猜想一:碳酸钙全部分解,剩余固体成分为_______。
做出该猜想的依据是(用化学方程式表示)_______,验证该猜想的方案为_______。
猜想二:碳酸钙部分分解,剩余固体成分为_______。
验证该猜想的方案如下表所示:
实验步骤 | 实验现象 | 结论 | |
步骤A | 将加热后的固体放入水中,搅拌、静置。 | 底部有大量白色不溶物 | 剩余固体中含有碳酸钙 |
步骤B | 取上层清液,滴加无色酚酞试液。 | 变红 | 剩余固体中含有_______ |
(反思与评价)同学们讨论后认为“猜想二”的验证方案存在问题,理由是(用化学方程式表示)_______。
【题目】下图中“—”表示相连的物质之间可以在溶液中发生化学反应。下列表中 四组选项中,符合该图要求的是( )
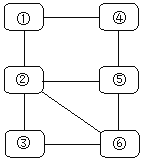
① | ② | ③ | ④ | ⑤ | ⑥ | |
A | 锌 | 稀盐酸 | 碳酸钙 | 硫酸铜 | 烧碱 | 硫酸铁 |
B | 铁 | 稀硫酸 | 氯化钡 | 硝酸铜 | 熟石灰 | 碳酸钠 |
C | 二氧化碳 | 氢氧化钠 | 稀硫酸 | 氢氧化钡 | 氯化铜 | 碳酸钾 |
D | 氧化钙 | 稀盐酸 | 铁 | 稀硫酸 | 碳酸钠 | 氢氧化钡 |
A.AB.BC.C
【题目】用科学方法认识和改造物质。请你参与探究并填空:按照科学认识的过程,科学方法主要蕴含在两个阶段:一是感性认识阶段,主要是为了获得证据,如观察、预测、实验等;二是理性认识(理性思维)阶段,主要是为了形成科学认识,如科学抽象、科学假说,像比较与对比、归纳与演绎等。在前一阶段的学习中,我们通过实验、观察等手段验证了很多化学反应的发生,运用了“归纳、演绎;比较、对比”等科学的一般方法认识了几种典型的酸、碱、盐。请你运用以上方法认识硫酸铜。
(1)用归纳/演绎的方法认识硫酸铜的化学性质已知下列反应:
H2SO4+BaCl2═BaSO4↓+2HClNa2SO4+BaCl2=BaSO4↓+2NaCl
MgSO4+BaCl2═BaSO4↓+MgCl2K2SO4+BaCl2=BaSO4↓+2KCl
①从微观分析这组反应能够发生的原因是_____。
②由①中得到的规律可以推论“硫酸铜溶液也能跟氯化钡溶液反应”,运用的是_____的方法.
(2)用实验的方法认识硫酸铜的化学性质首先验证(1)②中“硫酸铜溶液也能跟氯化钡溶液反应”的推论,需进行实验是:
实验操作 | 实验现象 | 结论 |
取少量硫酸铜溶液于A试管中,然后再滴加氯化钡溶液 | _____ | 结论:硫酸铜溶液能跟氯化钡溶液反应 |
②用实验的方法认识硫酸铜的其他性质
实验操作 | 实验现象 | 结论 |
取少量硫酸铜溶液于B试管中,然后再滴加2﹣3滴紫色石蕊试液,振荡 | 石蕊试液变红 | 结论:硫酸铜溶液显_____ |
取少量硫酸铜溶液于C试管中,然后再滴加氢氧化钠溶液 | _____ | 结论:_____ |
(3)用重要的学科实验方法——“化学转化法”改造物质人类利用化学变化,创造出我们所需要的物质,极大地促进了人类社会的发展。我们的祖先很早就掌握了多种炼铜工艺。
◆火法炼铜:将孔雀石(主要成分是Cu2(OH)2CO3)和木炭一起加热可以得到红色的金属铜,请写出上述反应的化学方程式:①_____。②_____。(友情提示:孔雀石受热易分解,得到氧化铜、二氧化碳和水;在加热的条件下木炭和氧化铜反应得到铜和二氧化碳。)
◆湿法炼铜:将天然铜的化合物进行湿法炼铜,先用硫酸与氧化铜反应,再用铁置换出铜。“曾青得铁则化为铜”,“曾青”指可溶性铜盐,即铜盐遇到铁,就有铜生成。请写出上述反应的化学方程式:①_____。②_____。(友情提示:先用硫酸与氧化铜反应得到可溶性铜盐;铜盐遇到铁就有铜生成。)