题目内容
【题目】某化学兴趣小组的同学对碳酸钙高温加热一段时间剩余固体的成分进行探究。
(提出问题)加热后剩余固体的成分是什么?
(猜想与探究)
猜想一:碳酸钙全部分解,剩余固体成分为_______。
做出该猜想的依据是(用化学方程式表示)_______,验证该猜想的方案为_______。
猜想二:碳酸钙部分分解,剩余固体成分为_______。
验证该猜想的方案如下表所示:
实验步骤 | 实验现象 | 结论 | |
步骤A | 将加热后的固体放入水中,搅拌、静置。 | 底部有大量白色不溶物 | 剩余固体中含有碳酸钙 |
步骤B | 取上层清液,滴加无色酚酞试液。 | 变红 | 剩余固体中含有_______ |
(反思与评价)同学们讨论后认为“猜想二”的验证方案存在问题,理由是(用化学方程式表示)_______。
【答案】氧化钙 CaCO3![]() CaO+CO2↑ 取样,滴加足量的稀盐酸,若无气泡产生,说明猜想一成立 氧化钙、碳酸钙 CaO CaO+H2O= Ca(OH)2
CaO+CO2↑ 取样,滴加足量的稀盐酸,若无气泡产生,说明猜想一成立 氧化钙、碳酸钙 CaO CaO+H2O= Ca(OH)2
【解析】
猜想一:碳酸钙能分解生成氧化钙和二氧化碳,若碳酸钙全部分解,则剩余的固体时氧化钙,要证明全部分解,则需要证明剩余的固体中不含有碳酸钙,而碳酸钙能与盐酸反应生成气体,故可以采用加入盐酸,观察到没有气体产生,证明猜想一正确,故填:氧化钙,CaCO3![]() CaO+CO2↑,取样,滴加足量的稀盐酸,若无气泡产生,说明猜想一成立;
CaO+CO2↑,取样,滴加足量的稀盐酸,若无气泡产生,说明猜想一成立;
猜想二:若碳酸钙部分分解,则所剩余的固体中含有氧化钙和碳酸钙,固体:氧化钙、碳酸钙;
氧化钙能与水反应生成氢氧化钙,氢氧化钙是微溶于水的物质,其水溶液呈碱性,能使酚酞试液变红,故观察到溶液变红,可以证明固体中含有氧化钙,故填:
实验步骤 | 实验现象 | 结论 | |
步骤A | 将加热后的固体放入水中,搅拌、静置. | 底部有大量白色不溶物 | 剩余固体中含有碳酸钙 |
步骤B | 取上层清液,滴加无色酚酞试液. | 变红 | 剩余固体中含有CaO |
由于氢氧化钙是微溶于水的物质,也就是设计的实验中出现白色不溶物也有可能是氢氧化钙,故实验二存在一定的问题,故填:CaO+H2O= Ca(OH)2.

【题目】现有25 g石灰石样品,请按下面要求计算:
(1)25 g样品与足量的稀盐酸反应放出8.8 gCO2(杂质不溶于酸,且不与酸反应),请计算该样品的纯度(CaCO3的质量分数)是多少________?
(2)若将一定质量的该石灰石样品高温煅烧,有关物质质量随反应时间的变化如表所示:
时间/min | t1 | t2 | t3 | t4 | t5 |
CO2质量/g | 2.2 | 4.4 | 6.6 | 8.8 | 8.8 |
剩余固体质量/g | 22.8 | 20.6 | m | 16.2 | 16.2 |
则m=_____,t3时剩余固体中除杂质外含有的物质是____(填化学式)。
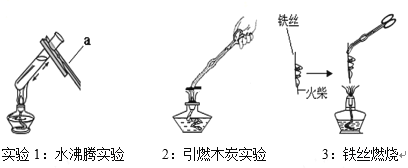
【题目】氧气是重要的资源,回答下列问题。
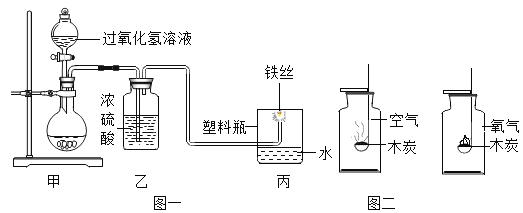
(1)图一为“铁丝在氧气中燃烧”的实验改进装置(浓硫酸具有吸水性,可干燥氧气)。图一甲装置:固体是二氧化锰,其作用是______________;发生反应的文字表达式为________;图一丙装置:铁丝在氧气中燃烧,观察到的实验现象_______________;用塑料瓶代替集气瓶的优点之一是_______。
(2)某兴趣小组为了研究用向上排空气法和排水法收集的氧气浓度是否有差异,做了如下实验:加热高锰酸钾固体,分别用两种方法各收集三瓶氧气,井使用传感器测定收集到的氧气浓度,数据见表。
收集方法 | 向上排空气法 | 排水集气法 | ||||
氧气浓度% | 79.6 | 79.7 | 79.9 | 90.0 | 89.8 | 89.3 |
氧气平均浓度% | 79.7 | 89.7 | ||||
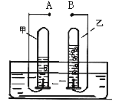
①用向上排空气法收集氧气时,以能使放置在集气瓶瓶口的带火星木条复燃为氧气集满的标准;用排水集气法收集氧气时,以观察到____________为氧气集满的标准。
②以上两种方法中,用_________________法收集到的氧气更纯净。
③不考虑操作因素,排水集气法获得的氧气体积分数不能达到100%主要原因_____________。
④向上排空气法收集到的氧气浓度只有80%左右的原因有_________(填字母序号)。
A 氧气的密度略大于空气的密度
B 加热高锰酸钾固体产生氧气的浓度只有80%左右
C 当观察到带火星木条复燃时,集气瓶内还有空气
D.当氧气进入集气瓶时,瓶内空气与进入的氧气相互扩散
(3)分别把点燃的木炭放入装有空气和氧气的集气瓶中燃烧,如图二,对比木炭在空气和氧气中燃烧的现象,说明影响燃烧剧烈程度的一种因素是________________。
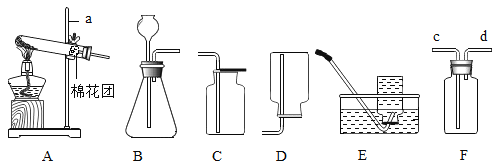
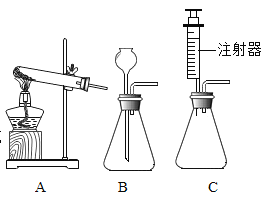
(4)在潜水艇中提供氧气的反应原理之一是:过氧化钠(固体)和水反应生成氢氧化钠和氧气,实验室中可用(如图三所示)_____ 装置来模拟其制取过程(填字母序号)。