题目内容
【题目】粗盐中除NaCl外还含有MgSO4以及泥沙等杂质。初步提纯粗盐的实验流程及相关物质的溶解度曲线如下图所示:
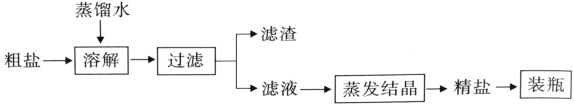
(1)滤液中含量最多的溶质是_______。
(2)玻璃棒在过滤时所起的作用是______。
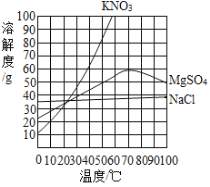
(3)本实验从滤液得到精盐,采用的是蒸发溶剂而不是降温的方法,结合右图说明其原因是_____。
(4)常温下,10mL蒸馏水最多可溶解NaCl的质量约为_____g(保留1位小数)。
(5)在温度约为_____℃时(取整数),MgSO4饱和溶液的溶质质量分数最大,此时结晶出的NaCl纯度较高。
【答案】氯化钠或NaCl 引流 氯化钠的溶解度受温度影响小 3.6 70
【解析】
(1)粗盐中的主要成分是氯化钠,故滤液中的含量最多的溶质是氯化钠。
(2)过滤时,玻璃棒起引流的作用。
(3)氯化钠的溶解度受温度影响小,而硫酸镁的溶解度随温度的变化较大,故采用蒸发结晶。
(4)由题意可知,常温下氯化钠的溶解度为36g,故10ml的水中最多能溶解氯化钠的质量为3.6g。
(5)由图可知,在70℃时,硫酸镁的溶解度最大,故在温度约为70℃时(取整数),MgSO4饱和溶液的溶质质量分数最大,此时结晶出的NaCl纯度较高。

 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案【题目】同学们在初中化学实验室中,发现一瓶如图所示久置的瓶口有白色固体、瓶塞丢失的无色溶液。已知原溶液可能是NaCl、NaOH或Na2CO3三种溶液中的一种,为确定溶液成分,同学们进行了如下探究:
(1)探究成分
①小张同学取待测液测得pH=10,他得出的关于溶液成分的结论是____。他取少量待测液于试管中,加入过量的稀HCl,看到_________,由此小张同学认为,溶液为Na2CO3溶液。
②小李同学对小张同学的结论提出疑问,拟进行了以下实验:取少量待测液于试管中,加入过量的BaCl2溶液,生成白色沉淀,该反应方程式为__________,过滤,取滤液,(写出还需进行的操作及现象)___________。通过实验,小李认为小张结论不正确。
③同学们通过讨论认为试剂瓶原标签应该是氢氧化钠,但因吸收空气中 ______的而变质。
(2)测定碳酸钠的浓度
取该试剂瓶中溶液50g倒入烧杯中,再向烧杯中逐滴滴加盐酸使其充分反应至无气泡产生(假设生成的二氧化碳全部逸出)。测得加入盐酸的质量与烧杯中的物质的质量关系如下表所示。
累计加入盐酸的质量/g | 0 | 25 | 37.5 | 50 |
烧杯中物质的总质量/g | 50 | 75 | 85.3 | 97.8 |
请你计算:
①这一测定过程中产生二氧化碳质量为_______g。
②这一瓶试剂中碳酸钠的质量分数_______(写出计算过程)。