��Ŀ����
����Ŀ���Ͻ�����Ҫ�Ľ�������.
��1��������Ʒ��ʹ�õ���Ҫ�������ںϽ����_____��
A���ƿ B����ͧ C����ֹ�
��2�������dz����ĺϽ���������_____������������
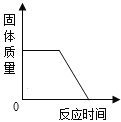
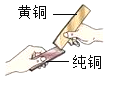
��3����ͭ��ͭп�Ͻ𣬽���ͭƬ�ͻ�ͭƬ����̻�����ͼ��ʾ������ͭƬ���������ԵĻ��ۣ�˵��_____.
��4����ͭ������Ҫ��Zn��ZnO��Cu��CuO,����Ϊ���ʣ�������ͭ���ɵõ�����п������Ҫ�������£����ʲ�����ˮ�����μӷ�Ӧ����

����˵����ȷ����_____;
A ���еIJ�������������
B ��ҺAһ��Ϊ��ɫ
C ��ҺA������С����ҺB.
���𰸡�C ����� ��ͭ��Ӳ�ȱȴ�ͭ��Ӳ�ȴ� AC
��������
(1)A�����ƿ�����������ƶ��ɵģ��������ǽ������ϣ��ʲ��������⣻
B������ͧ���úϳ����Ƴɵģ��ϳ�����������ϳɲ���֮һ�ʲ��������⣻
C������ֹ����ò�����Ƴɵģ������ĺϽ𣬹ʷ������⡣
��ѡC
(2)����������̼�ĺϽ���Ҫ�ɷ����������ڻ�����������
(3)����ͭƬ�ͻ�ͭƬ����̻�����ͭƬ���������ԵĻ��ۣ�˵����ͭ��Ӳ�ȱȴ�ͭ��Ӳ�ȴ����ͭ��Ӳ�ȱȴ�ͭ��Ӳ�ȴ�
(4)��ͭ���м��������ϡ����õ���ҺA������ͭ������п�����ټ��������п��Cu2+�û��������õ���ҺB������Ũ�������½ᾧ�õ�����п�ľ��塣
A�����еIJ������������ˣ���Ѳ���ϡ��������ʳ�ȥ������û�������ͭ���ʹ��˵����ʷ������⡣
B����ҺA����ͭ���ӣ�Ϊ��ɫ���ʲ��������⣻
C��п��ͭ����ҺA���û�������п�ĺ�ͭ��1:1�ĸ����ȷ�Ӧ��������65:64���ʷ�Ӧ����Һ�����������ҺA������С����ҺB���ʷ������⡣
��ѡ��AC

����Ŀ����ͼ1����ʯ��ʯΪԭ���Ʊ��ߴ���ϸ̼��ƵĹ�������ͼ��
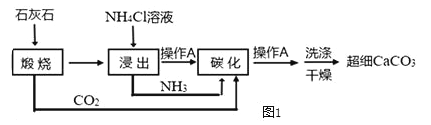
��1�������в���A������_____��ʵ������ò����õ��IJ����������ձ���_____��_____��
��2����Ҫ��Ӧԭ����
�������������裺��Ҫ��Ӧ�Ļ�ѧ����ʽΪ_____����Ӧ��������Ϊ_____��Ӧ��
�������������裺CaO+2NH4Cl��CaCl2+H2O+2NH3����
����̼�������裺CO2+2NH3+H2O+CaCl2��CaCO3��+2 NH4Cl��
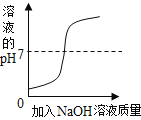
��3������ʯ��ʯ�õ��Ĺ����У�����CaO�⣬����������MgO��FeO�����ʣ���������������Ϊ��֤����þ�����ʲ�����������Ҫ�ʵ������Һ��pH�����ݷ�Ӧ�ڼ�����ĸ�隣ȣ��μӷ�Ӧ�������ƺ��Ȼ�淋������ȣ�Ϊ_____����ʵ����������Ѹ�隣�Ҫ�Ը�����һ��ֵ��ԭ����_____��
��4�����������̿�ѭ��ʹ�õ����ʳ���H2O��CO2��NH3֮�⣬����_____��
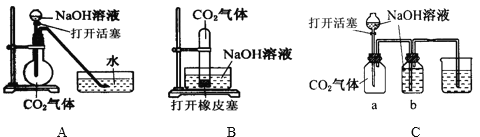
��5��ʵ��������ͼ2װ����ģ�����������Ʊ��ߴ���ϸ̼��ƣ�
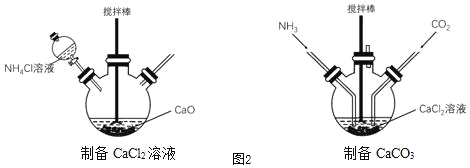
�ٽ����������_____��
���Ʊ�CaCl2��Һʱ��Ҫ��װ�ü��ȣ���Ҫ������_____��
A �ӿ췴Ӧ���� B �ٽ������ݳ�
����֪�ڳ��º�һ��������ѹ�£�CO2��NH3��100gˮ�зֱ����ܽ�0.169g��52.9g���Ʊ�CaCO3ʱӦ��ͨ�백����ͨ�������̼��������_____��
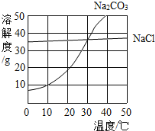
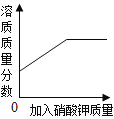
�ܽ�ȡһ����NH4Cl��Һ��������������ֱ��Ӱ��������CaCl2��Һ����������������֪0��100��ʱNH4Cl���ܽ�����±���
�¶ȣ��棩 | 0 | 20 | 40 | 60 | 80 | 100 |
�ܽ⣨g�� | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 |
�����200g 80��ʱNH4Cl�ı�����Һ�봿������ǡ����ȫ��Ӧ�������ַ�Ӧ��õ�CaCl2������_____����д��������̣�����һλС������
����Ŀ��ÿ��4��5�·���У���и߷��ڣ�Ϊ��ѧУ����ijƷ�ƶ�����������Һ�����Ϊ������Һ�IJ�����Ϣ��
�������ȣ�ClO2��1000mL | |
������������ | 80% |
�� �� | 1.2g/ml |
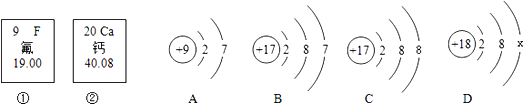
��1���������ȣ�ClO2������Ԫ�صĻ��ϼ���_____��
��2��ΪԤ�����У�ijУҽ����Ա����ϡ����20%��ȫУ���ҽ���ȫ����������Ԥ����Ⱦ���ĽǶȿ���������_____��ѡ�����ƴ�ȾԴ�������жϴ���;����������������Ⱥ������
��3�����й��ڶ������ȣ�ClO2����˵����ȷ����_____��
A��������������Ԫ�غ���Ԫ�����
B�����������ɶ������ȷ��ӹ���
C.1���������ȷ�����1����ԭ�Ӻ�1�������ӹ���
D��������������Ԫ�����������������ʽΪCl%��![]() ��100%
��100%
��4��������40kg��������Ϊ20%��ϡ������������Һ����Ҫ���ֶ�����������Һ_____kg��
��5������������֢ʱ����ַ�������������������ϸ����ɱ�����ʵ�ת�Ƶ���֢����������ԭ��Ĺ������˹�������_____ ��ѡ������������������������������������