题目内容
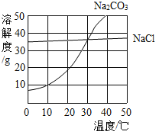
【题目】如图是氯化钠、碳酸钠和氢氧化钙的溶解度曲线
![]()
(1)碳酸钠和氯化钠的溶解度相等时对应的温度是__________。
(2)20℃时,分别向50g水中加入15g氯化钠和碳酸钠,充分溶解后形成饱和溶液的是______。
(3)将氢氧化钙的饱和溶液转化成不饱和溶液的方法是_______________________。
(4)碳酸钠中混有少量的氯化讷,可以用_____________的方法得到碳酸钠晶体
【答案】30℃ 碳酸钠 加入溶剂水(或降低温度) 降温结晶
【解析】
(1)由溶解度曲线可知,碳酸钠和氯化钠的溶解度相等时对应的温度是30℃。
(2)20℃时,氯化钠和碳酸钠的溶解度分别约是36g、20g,则50g水中最多能溶解氯化钠和碳酸钠的质量分别为18g、10g,所以向50g水中加入15g氯化钠和碳酸钠,充分溶解后能形成饱和溶液的是碳酸钠。
(3)氢氧化钙的溶解度随温度的升高而减小,降低温度,氢氧化钙的溶解度变大,所以将氢氧化钙的饱和溶液转化成不饱和溶液的方法有加入溶剂水、降低温度。
(4)碳酸钠的溶解度受温度影响较大,对于溶解度受温度影响较大的物质,采用降温结晶法使溶质结晶析出。

练习册系列答案
相关题目