题目内容
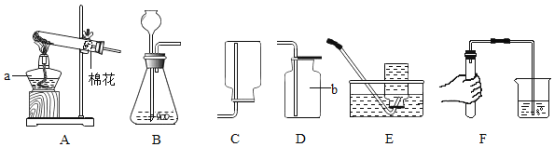
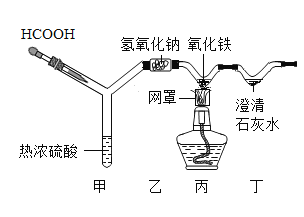
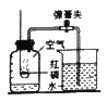
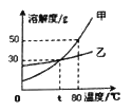
【题目】化学是一门以实验为基础的科学。请结合图示回答以下问题:
常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。
(1)试管尾部放一团湿棉花的目的是_________。
(2)用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。说明生成的气体是____。
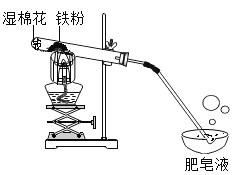
(3)探究试管中剩余固体成分是什么?
(查阅资料)
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
(初步验证)试管中剩余固体为黑色,能全部被磁铁吸引。
(猜想与假设)猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是________。
(实验探究)
实验操作 | 实验现象 | 实验结论 |
取少量样品于试管中,加入足量稀盐酸,观察现象 | ___________ | 猜想二正确 |
(实验结论)铁和水蒸气反应的化学方程式为__________。
(反思与交流)该黑色固体不可能是Fe2O3,理由是__________。
【答案】提供水蒸气 氢气 Fe3O4 无气泡产生 3Fe+4H2O![]() Fe3O4+4H2↑ 氧化铁不能被磁铁吸引(或氧化铁为红棕色粉末)
Fe3O4+4H2↑ 氧化铁不能被磁铁吸引(或氧化铁为红棕色粉末)
【解析】
(1)试管尾部放一团湿棉花的目的是提供水蒸气。
(2)反应中有肥皂泡飘到空中,说明气体密度比空气小,用燃着的木条靠近肥皂泡,有听到爆鸣声,说明气体具有可燃性,说明生成的气体是氢气。
(3)猜想与假设:
因为试管中剩余固体为黑色,能全部被磁铁吸引。根据资料FeO、Fe3O4为黑色。所以猜想一:铁有部分剩余,剩余固体是Fe与Fe3O4;猜想二:铁全部反应完全,剩余固体是Fe3O4。
实验探究:
实验操作:取少量剩余固体于试管中,加入足量稀盐酸;
实验现象及结论:铁和稀盐酸反应生成氯化亚铁和氢气,四氧化三铁和稀盐酸反应生成氯化铁和氯化亚铁和水;如果固体全部溶解,产生气泡,说明剩余固体是铁和四氧化三铁,猜想一成立;如果剩余固体全部溶解,不产生气泡,说明剩余固体是四氧化三铁,猜想二成立。
实验结论:
铁和水蒸气反应生成四氧化三铁和氢气,化学方程式为3Fe+4H2O![]() Fe3O4+4H2↑。
Fe3O4+4H2↑。
反思与交流:
该黑色固体不能是Fe2O3,理由是Fe2O3是红棕色粉末且不能被磁铁吸引。

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案