题目内容
【题目】下列图象不能正确反映对应变化关系的是( )
A.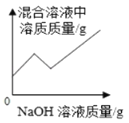 向硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液
向硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液
B.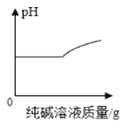 向氯化钙溶液中滴加纯碱溶液
向氯化钙溶液中滴加纯碱溶液
C.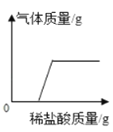 向碳酸钠和氢氧化钠的混合溶液中滴加盐酸
向碳酸钠和氢氧化钠的混合溶液中滴加盐酸
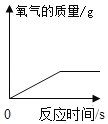
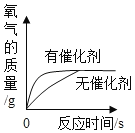
D.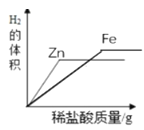 向等量的镁粉和铁粉中加稀盐酸
向等量的镁粉和铁粉中加稀盐酸
【答案】D
【解析】
A、向硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液,酸和碱优先发生中和,当氢氧化钠将硫酸消耗尽后,氢氧化钠和硫酸铜发生化学反应,生成氢氧化铜沉淀和硫酸钠。所以溶液中溶质的变化分为三个阶段:增长(氢氧化钠和硫酸发生中和反应)、减小(氢氧化钠和硫酸铜反应生成难溶于水的氢氧化铜沉淀和硫酸钠)、增大(滴加氢氧化钠至过量)。故A正确;
B、向氯化钙中滴加纯碱,纯碱是碳酸钠,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠。且碳酸钠的水溶液呈碱性。在初始状态,氯化钙和生成的氯化钠呈中性,所以溶液pH值不变,当纯碱溶液过量,溶液中碱性增强,pH值增大。故B正确;
C、向碳酸钠和氢氧化钠溶液中加入稀盐酸,稀盐酸优先和氢氧化钠发生中和反应,当稀盐酸将混合溶液中的氢氧化钠溶液消耗尽后,稀盐酸和碳酸钠反应生成二氧化碳气体。所以在滴加的过程中,溶液最开始不产生气体,之后产生气体。故C正确;
D、等质量的镁粉和铁粉中加入稀盐酸。镁的相对原子质量是24,而铁的相对原子质量是56。根据化学方程式可知(Mg+2HCl=MgCl2+H2、Fe+2HCl=FeCl2+H2),当镁和铁的质量相等时,镁产生的氢气的量较多。而且铁的金属活动性顺序比铁强。所以图像应该是镁对应的直线产生氢气多,并且陡峭,铁对应的直线产生的氢气少,并且平缓。故D错误。
故选D。

【题目】碳酸钡广泛应用于显像管(CRT)、陶瓷、光学玻璃等行业。有一种碳酸盐矿石其主要成分为碳酸钡和碳酸钙,以此矿石为原料生产碳酸钡的流程如下图所示。
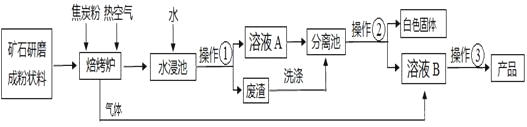
(已知):碳酸钡和碳酸钙具有相似的化学性质,高温下能分解成两种氧化物;氧化钡和氧化钙都能与水反应生成对应的氢氧化物,这两种氢氧化物均可以和二氧化碳反应。但氢氧化物溶解度有一定的差异,下表所示的是两种氢氧化物在不同温度下的溶解度。
温度/℃ | 0 | 40 | 80 |
Ca(OH)2溶解度/g | 0.187 | 0.141 | 0.094 |
Ba(OH)2溶解度/g | 1.67 | 8.22 | 101.4 |
(1)写出焙烧炉中含钡元素物质发生反应的化学方程式: ;
(2)除了水之外,进入分离池中的物质是 和 ,请你推测分离池中操作②的方法是 (选填“A”或“B”)。
A.降温,过滤; B.加热,过滤
(3)写出由溶液B制取产品的化学方程式: ;
(4)以下相关说法正确的是 。
A.对矿石进行预处理“研磨成粉状”有利于充分反应
B.焙烧炉中添加焦炭粉和热空气是为了维持炉内的高温状态
C.焙烧炉内只涉及分解反应
D.废渣需要经过洗涤才能弃渣,是为了保护环境,同时充分利用原料