题目内容
【题目】探究氯酸钾和二氧化锰制氧气实验中反应物与催化剂的最佳质量比.
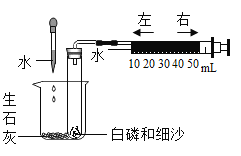
实验中采用图1实验装置,取20g氯酸钾,分成10等份,每份2g,分别装入10支试管中.在10支试管中分别加入不同质量的二氧化锰,分别测量二氧化锰与氯酸钾在不同质量比时,生成200ml氧气所消耗的时间.实验记录的数据如下:
实验编号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
二氧化锰的质量(g) | 0.1 | 0.2 | 0.33 | 0.4 | 0.5 | 0.66 | 1 | 1.3 | 2 | 3 |
二氧化锰与氯酸钾的质量比 | 1:20 | 1:10 | 1:6 | 1:5 | 1:4 | 1:3 | 1:2 | 2:3 | 1:1 | 3:2 |
生成200ml氧气时间(秒) | 235 | 186 | 162 | 147 | 133 | 117 | 143 | 160 | 211 | 244 |
请回答下列问题:
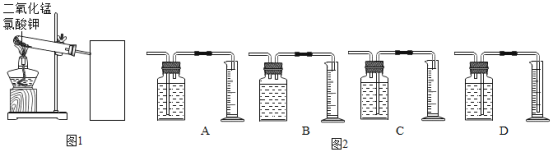
(1)为完成本实验,方框内应选择图2气体收集装置中的是_____(选填序号)该收集利用了氧气的_____性质.收集气体前集气瓶内未装满水,对实验结果_____(填“有”或“没有”)影响.
(2)分析上述数据,你认为利用此法制氧气,二氧化锰与氯酸钾的最佳质量比为_____.
(3)利用双氧水和二氧化锰的混合物制氧气比加热氯酸钾和二氧化锰混合物制氧气更好,请写出前者的两个优点①_____②
(4)催化剂能影响化学反应速度,温度、反应物的浓度、接触面积等也会对化学反应速度带来影响.分析上表数据,结合影响化学反应速度的
①当二氧化锰与氯酸钾的质量比高于最佳质量比时,反应速度变低的原因是_____.
②当二氧化锰与氯酸钾的质量比低于最佳质量比时,反应速度变低的原因是_____.
【答案】D; 不易溶于水; 没有 1:3; 节能;更安全;更环保;价格低廉,操作简便等; 二氧化锰用量多,导致反应物氯酸钾的质量分数变小 二氧化锰用量少,导致氯酸钾与二氧化锰的接触面积变小
【解析】
(1)要用排水取气法收集氧气,应短进长出,要保证压力平衡应选用D装置;利用排水装置收集的气体应具备的性质是难溶于水;空气不易溶于水,那么排出水的气体即为所收集的气体体积;
(2)通过观察图表中的数据可知,二氧化锰与氯酸钾的质量比是1:3时,所用的时间最少,反应速率最快;
(3)(4)双氧水和二氧化锰混合制氧气不需加热,可以节能,同时更安全;副产物是水无污染,更环保;价格低廉,操作简便等;
(4)①二氧化锰用量过多氯酸钾的质量分数就降低了,反应物的接触面积就少了,就影响了反应速度;
②反应速度的影响因素主要是反应物的接触面积,接触面积越大反应速度就越快,二氧化锰的用量过少与氯酸钾的接触面积就越小,所以反应速度慢。

 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案【题目】碳酸钙是钙片的主要原料.右图是某钙片说明书上的部分内容.兴趣小组的同学为了测定该钙片说明书上有关碳酸钙含量标注是否属实,进行了如下实验:取出4片片剂,研碎后放入烧杯中,加入过量的稀盐酸,同时测量6分钟(min)内生成CO2质量,测量数据如下表:(假定钙片中其它成分不与盐酸反应)
时间/min | 1 | 2 | 3 | 4 | 5 | 6 |
生成CO2的质量/g | 1.0 | 1.8 | 2.0 | 2.2 | M | 2.2 |
请回答:

(1)上表中M的数值是_____.
(2)根据计算判断该钙片说明书上有关碳酸钙含量标注是否属实_____.
【题目】(5分)KNO3和NaCl在不同温度时的溶解度如下表所示。请回答下列问题:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |||||||||
溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | ||||||||
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | |||||||||
(1)依据上表数据,绘制出KNO3和NaCl的溶解度曲线如图所示:
图中能表示KNO3溶解度曲线的是 (填“A”或“B”)

(2)由表中数据分析可知,KNO3和NaCl在某一温度时具有相同的溶解 度,则温度的范围是 ;
(3)某兴趣小组做了一下实验:
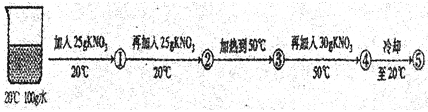
上述实验过程中得到的溶液一定属于不饱和溶液的是 (填数字序号),将⑤继续冷却至10℃,过滤,共可回收得到KNO3固体 g;
(4)硝酸钾中含有少量氯化钠时,可通过 (填“蒸发结晶”或“降温结晶”)的方法提纯。