题目内容
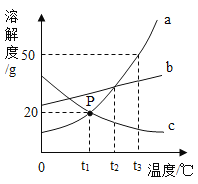
【题目】如图是A、B、C三种物质的溶解度曲线请认真分析并回答:
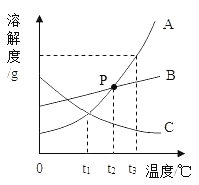
(1)t3℃时,A、B、C三种物质的溶解度由小到大的顺序为__________。
(2)t2℃时,A、B、C三种物质的饱和溶液降温到t1℃时变为不饱和溶液的是________。
(3) P点表示的含义是_______。
(4)当A中含有少量的B,可采用_______(填“降温”或“蒸发”)结晶的方法提纯A物质。
(5)t3℃时,若用A、B两物质各50g配成饱和溶液,则所需加水的质量A_______B(填“>”,“<”或“=”)。
【答案】C<B<A C 在t2℃时,物质A与B的溶解度相同 降温 <
【解析】
(1)结合三种物质的溶解度曲线图可知,t3℃时,A、B、C三种物质的溶解度由小到大的顺序是C<B<A。
(2)从溶解度曲线上可以得出,A、B溶解度随温度降低而减小,C物质的溶解度随温度降低而增大,所以在温度有t2℃降低为t1℃时,C将会由饱和溶液变为不饱和溶液。故选C。
(3)t2℃时,A、B溶解度曲线交于P点,故P点的含义是:在t2℃时,A和B的溶解度相等。
(4)从溶解度曲线上可以看出,A的溶解度受温度变化影响较大,而B的溶解度受温度变化影响较小,所以通过降温结晶方法可以提纯的物质为A。
(5)t3℃时,A物质的溶解度大,B物质的溶解度小,所以将等质量的A、B两物质配成饱和溶液,所需水质量的大小顺序是:A<B。

 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案【题目】小明想测定部分变质的熟石灰样品中Ca(OH)2的质量分数,他称取0.5g该样品,加足量水使之充分溶解,搅拌过滤后,在滤液中加入10%盐酸溶液,加入盐酸溶液的质量和溶液的pH见表。
加入盐酸溶液的质量/g | 0 | 2.5 | 3.65 | 6 |
溶液的pH | 12 | 11 | 7 | 2 |
(1)当pH=2时,溶液中所含的溶质是_____(写化学式)。
(2)求样品中Ca(OH)2的质量分数_____。(写出计算过程)