题目内容
【题目】多角度认识物质能帮助我们更全面地了解物质世界.以金属为例回答下列问题:
(1)认识金属元素的存在
①地壳中含量最多的金属元素是__.在自然界中,大多数金属以化合物的形态存在,而金、铂却能以单质形态存在,这是因为__.
②常见铁矿石有:赤铁矿(主要成分Fe2O3)、磁铁矿(主要成分Fe3O4)等.这两种铁矿石的主要成分含铁元素质量分数较大的是__.
(2)认识金属的性质
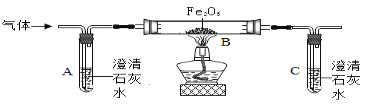
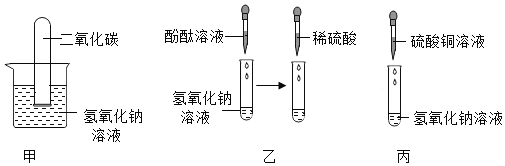
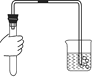
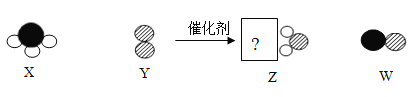
探究金属化学性质的实验如图所示:
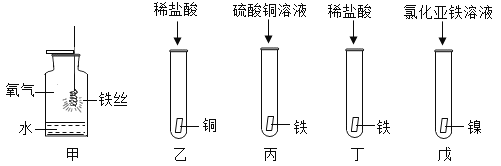
①进行如图甲实验时,瓶里放少量水的作用是__.
②图中只有乙实验没有明显现象,由此得出铜、铁、镍(Ni)及氢元素在金属活动性顺序中的位置关系,活动性由强到弱的顺序是__(填元素符号).
③写出如图丙实验反应的化学方程式__.
(3)认识金属的制备
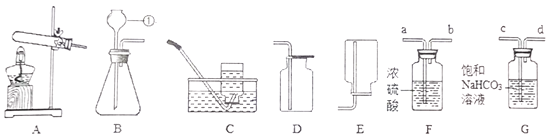
工业上,金属钨(W)可由氢气和三氧化钨(WO3)在高温下反应制得.写出反应的化学方程式:__;
(4)认识金属的用途
使用下列金属制品时,主要利用了金属导热性的是__(填标号).
A烤制食物时用的铝箔 B铜导线
C不锈钢高压锅 D黄金首饰
【答案】铝(或Al) 金、铂的化学性质很不活泼 Fe3O4 防止溅落的熔化物炸裂瓶底 Ni、Fe、H、Cu Fe+CuSO4=FeSO4+Cu WO3+3H2![]() 3H2O+W AC
3H2O+W AC
【解析】
(1)①地壳里各元素的含量前四位由多到少的顺序排列依次是氧,硅,铝,铁,因此地壳中含量最多的金属元素是Al;金、铂的化学性质很不活泼,所以在自然界中有单质存在;故填:铝(或Al),金、铂的化学性质很不活泼。
②Fe2O3中铁元素的质量分数:![]() ,Fe3O4中铁元素的质量分数:
,Fe3O4中铁元素的质量分数:![]() ,Fe3O4中铁元素的质量分数较大。故填:Fe3O4。
,Fe3O4中铁元素的质量分数较大。故填:Fe3O4。
(2)①铁丝燃烧实验中,集气瓶底预先放少量水的作用是防止生成的高温熔融物溅落从而炸裂集气瓶;故填:防止溅落的熔化物炸裂瓶底。
②由题干信息可知,镍能置换出铁,说明镍比铁活泼,铁能与稀盐酸反应置换出氢气,说明铁在氢之前,铜不能与稀盐酸反应,说明铜在氢之后,由此得出铜、铁、镍(Ni)及氢元素在金属活动性顺序是镍、铁、氢、铜。故填:Ni、Fe、H、Cu。
③铁与硫酸铜发生置换反应生成硫酸亚铁和铜。故填:Fe+CuSO4=FeSO4+Cu。
(3)三氧化钨与氢气在高温的条件下反应生成金属钨和水,故填:WO3+3H2![]() 3H2O+W;
3H2O+W;
(4)A、烤制食物时用的铝箔,是利用了金属铝的导热性;
B、铜作为导线,利用了金属的导电性;
C、不锈钢高压锅,利用了金属的导热性;
D、黄金首饰,利用了金具有黄色的金属光泽,且不化学性质稳定。
故选:AC。

【题目】“84”消毒液在新冠肺炎预防措施中使用较为广泛,其还具有漂白、杀菌、消毒的功效。某化学兴趣小组对 一瓶敞口久置的“84”消毒液的成分产生兴趣,在老师的指导下,展开探究。
已知:“84”消毒液和洁厕灵作用会产生氯气。
(提出问题)该敞口久置的消毒液中溶质有哪些?
(查阅资料)“84”消毒液的主要成分是次氯酸钠(NaClO)和氯化钠;NaClO 为有效成分,有腐蚀性并 易与空气中的 CO2 反应(2NaClO+CO2+H2O==2HClO+Na2CO3)。NaClO溶液、HClO都具有漂白、杀菌、消毒功效。HClO 不稳定,受热或光照条件下会发生分解。
(分析讨论)小组同学经过讨论,认为该消毒液中的溶质一定有____________________,可能还有 NaClO、Na2CO3、HClO中的一种或多种。
(实验探究)
实验操作 | 实验现象 | 实验结论 |
Ⅰ.向装入红色布条的试管中加入适量该消毒液 | 布条长时间不褪色 | 消毒液中不含___________ |
Ⅱ.另取少量该消毒液于试管中,滴入氯化钡溶液 | 白色沉淀 | 消毒液中含__________,发生反应的化学方程式为 ________ 。 |
(交流反思)生活中,“84”消毒液贮藏时应注意________________;一般不用“84”消毒液对蔬菜、水果进行消毒,其原因可能是________________。
(拓展延伸)
(1)次氯酸钠与稀硫酸可发生复分解反应,化学方程式为 __________________。
(2)“84”消毒液______(“能”或“不能”)与洁厕灵混合使用。