��Ŀ����
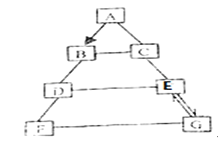
����Ŀ��X��Y��Z��W��Ϊ������Ԫ�أ�������Ԫ�����ڱ��е�λ����ͼ��ʾ����ش��������⣺
X | Y | ||||||
Z | W | ||||||
��1��X���γɶ��ֵ��ʣ�д���������ֵ��ʵ�����_____��
��2��ZԪ�ص�ԭ�ӽṹʾ��ͼ��_____��
��3��Ԫ�صķǽ�����Ϊ��ԭ�ӵĵõ�����������Y______W������ڡ���С�ڡ�����
��4��Wλ�����ڱ���_____���ڣ�_____���壬��Ԫ������������Ӧˮ����Ļ�ѧʽ��_____��������Ԫ�ؿ�����ĸW��ʾ��
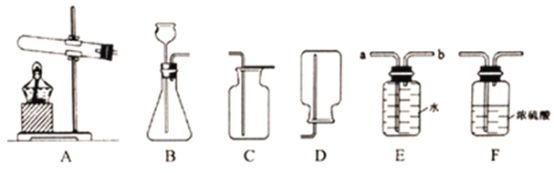
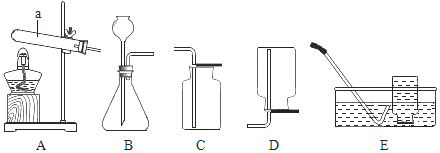
��5����̼����������ָͨ��һ���ķ���������ҵ�����в�����CO2����������д�������á�������NaOH��Һ��������CO2��������ͼ��ʾ����������������δ�������

����ݡ�����CO2����ͼ�ش����⣺
�ټ���A���ʵĻ�ѧʽ��_____������������������_____��
�ڿ�ѭ�����õ�B������һ�����е�������_____��
�۸ù����л���ѭ�����õ�������_____��
���𰸡����ʯ��ʯī�� C60 ��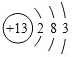 ������VI��д 6 ����Ҳ�ɣ�H2WO4Ca(OH)2��CaO�����ˣ�NaOH��CaO��
������VI��д 6 ����Ҳ�ɣ�H2WO4Ca(OH)2��CaO�����ˣ�NaOH��CaO��
��������
���⿼������1��Ԫ�����ڱ����ص㼰��Ӧ������2���ٸ�����ʯ����ˮ��������������ƣ�����������̼���Ʒ�Ӧ����̼��Ƴ������ǣ�����Һ���벻����Һ��Ĺ�����뷽�����ڸ���̼�������������Ʒ�Ӧ��������ǣ��۸���ѭ�����õ�������ָ��ǰ��ķ�Ӧ���Ƿ�Ӧ�����ķ�Ӧ������������
��1������Ԫ�����ڱ���֪��Xλ�ڵڶ����ڣ������壬X��̼��̼Ԫ�����γɶ��ֵ��ʣ����ʯ��ʯī�� C60�ȣ�
��2������Ԫ�����ڱ���֪��Zλ�ڵ������ڣ������壬ZԪ������Ԫ�أ�ԭ�ӽṹʾ��ͼ��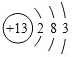 ��
��
��3������Ԫ�����ڱ���֪��Yλ�ڵڶ����ڣ������壬YԪ���Ƿ�Ԫ�أ�����������Ϊ7��Wλ�ڵ������ڣ�VI���壬WԪ������Ԫ�أ�����������Ϊ6����ԭ�ӱ���ԭ�Ӹ����õ����ӣ���Ԫ�صķǽ�����Ϊ��ԭ�ӵĵõ�����������Y����W��
��4��������Ԫ�����ڱ���֪��W λ�����ڱ��������ڣ�VI��д 6 ����Ҳ�ɣ����壬WԪ������Ԫ������Ԫ���������������������Ӧˮ���������ᣬ��ѧʽ��H2WO4��
��5�����ڲ��������������������̼��Ӧ����̼���ƣ����뷴Ӧ�������Լ����A������̼���Ʒ�Ӧ�������������������ܷų�������̼����������ˮ��Ӧ�����������ƣ�����������̼���Ʒ�Ӧ�����������ƺ�̼��ƣ�̼��Ƹ��·ֽ����������ƺͶ�����̼������A���ʿ����������ƻ������ƣ���ѧʽ��Ca(OH)2��CaO������������ǽ������Һ����룬���������ķ����ǹ��ˣ�
�ڷ�Ӧ���еķ�Ӧ��̼�������������Ʒ�Ӧ����̼��Ƴ������������ƣ������������Dz����еķ�Ӧ������������ƿ���ѭ�����ã����̼�������������Ʒ�Ӧʱ��̼���ƹ����������ܺ���̼���ƣ�����������ƹ����������������ƣ����Կ�ѭ�����õ� B ������һ�����е�������NaOH��
���������̼��Ƹ������������ƺͶ�����̼��ǰ������A�����������ƣ����������ƻ���ѭ�����á�

 �Ķ��쳵ϵ�д�
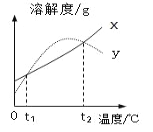
�Ķ��쳵ϵ�д�����Ŀ��NH4Cl��Na2SO4���ܽ�ȱ����ܽ��������ͼ������˵���������( )

�¶�/�� | 10 | 20 | 30 | 40 | 50 | 60 | |
�ܽ��S/g | NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 60.2 |
Na2SO4 | 9.6 | 20.2 | 40.8 | 48.4 | 47.5 | 47.0 | |
A. ��ΪNH4Cl
B. t3Ӧ����40����50��
C. 55��ʱ���ֱ���������Һ������������ˮ���õ����������ף���
D. �������ļס��ұ�����Һ��t3���µ�t1�������ľ����������