题目内容
【题目】矿物质水中元素及其国标含量如表所示.请回答下列问题:
矿物质水中主要成分 | |
偏硅酸 硫酸根 氯离子 | 钙 钠 钾 镁 |
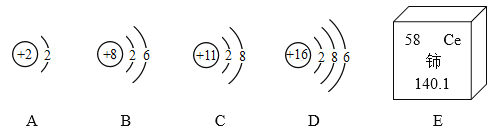
(1)矿物质水中含有________种非金属元素;
(2)久置的水中会溶有一定量的氧气.请写出两个氧分子的符号:________;
(3)写出表中的一种阴离子符号:________;
(4)偏硅酸![]() 中硅元素的化合价为________价.
中硅元素的化合价为________价.
【答案】![]() 2O2
2O2 ![]() (或
(或![]() 或
或![]() )
) ![]()
【解析】
(1)由矿物质水中主要成分可知,矿物质水中含有种非金属元素有硅、硫、氢、氧、氯5种元素;
(2)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则两个氧分子可表示为:2O2.
(3)带负电的原子或原子团为阴离子,故表中的阴离子有硫酸根离子、氯离子、亚硫酸根离子等,其符号为:![]() (或
(或![]() 或
或![]() );
);
(4)根据在化合物中正负化合价代数和为零,设偏硅酸中硅元素的化合价为x,则:
(+1)×2+x+(-2)×3=0,则x=+4。

【题目】兴趣小组同学为了测定某中碳酸钙的质量分数,称取25.0g珍珠粉样品,进行四次高温煅烧、冷却、称量剩余固体的重复操作(杂质不参加反应),记录数据如下:
操作次数 | 第1次 | 第2次 | 第3次 | 第4次 |
剩余固体质量(g) | 21.6 | 19.2 | 16.2 | 16.2 |
试计算:
(1)完全反应后生成二氧化碳的质量是__g。
(2)求珍珠粉中碳酸钙的质量分数。(写出计算过程)__________.
【题目】金属镁可与热水反应生成氢氧化镁和氢气,所得溶液呈碱性,可使酚酞溶液显紅色。某同学将镁条放在水中煮沸,趁热取出部分溶液,滴加酚酞溶液,变为红色,放置在空气中一段时间后,发现溶液的红色褪去了。
(1)镁与热水反应的化学方程式是_______。
(2)查阅资料:溶液红色褪去的原因是溶液碱性减弱。
(提出问题)导致溶液碱性减弱的原因是什么?
(假设与分析)
假设1:可能是氢氧化镁与N2或O2发生了反应。
假设2:可能是溶液吸收了空气中的二氧化碳。
假设3:可能是氢氧化镁的溶解度随温度的降低而_____。
由碱的性质可知,假设1不成立。
(实验探究)
实验操作 | 实验现象 | 结论 |
1.取上述红色溶液,保持温度不变,在空气中放置一段时间,观察现象。 | _______ | 假设2成立 |
2.取上述红色溶液,_______观察现象。 | 红色褪去 | 假设3成立 |
(拓展延伸)
(3)将一小块金属钠投入硫酸铜溶液时,产生蓝色沉淀。请解释其原因:_________。
(4)除上述金属外,根据金属活动性顺序,预测_____也能跟硫酸铜溶液反应产生上述现象(举一例即可)。