题目内容
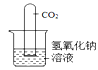
【题目】实验室用石灰水而不用氢氧化钠溶液鉴定二氧化碳。氢氧化钠能否与二氧化碳反应?
(查阅资料)(1).氢氧化钠溶液与二氧化碳反应生成易溶的碳酸钠,碳酸钠在二氧化碳过量的条件下继续与水和二氧化碳反应生成碳酸氢钠
(2).碳酸钠和碳酸氢钠性质对比如下表
操作 | NaHCO3溶液 | Na2CO3溶液 |
加入稀盐酸 | 产生气泡 | 产生气泡 |
加入稀CaCl2溶液 | 无明显变化 | __________________(填写现象) |
加热溶液至沸腾,并将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
(进行实验)
实验操作 | 化学方程式 | 结论及实验现象 |
| ____________ | 氢氧化钠与二氧化碳反应生成碳酸钠,写出该反应化学方程式:_________________ |
(实验反思)学习小组同学经过分析讨论,认为产生此实验现象的原因可能有两种:
一种是NaOH与CO2发生了反应; 另一种是_______________________
(2) 为了进一步验证CO2与NaOH溶液已经发生反应,请你设计一个简单的实验检验生成的新物质。
实验步骤 | 实验现象 | 解释与结论 |
_________ | _____________ | NaOH与CO2发生了反应 |
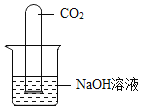
(实验拓展)该小组同学将二氧化碳通入氢氧化钠溶液中,利用数字化技术测定溶液pH值变化,待完全反应后,观察到溶液中逸出大量气泡,pH出现两段S型变化曲线。
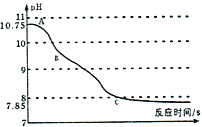
(实验分析)
(3)AB段变化的原因可能是______________。
BC段变化的原因可能是______________。
实验操作为________________。
实验现象是_________________。
【答案】产生白色沉淀 试管内液面上升 CO2+2NaOH═Na2CO3+H2O 二氧化碳溶于水 向溶液中加入足量的稀盐酸 产生气泡 二氧化碳和氢氧化钠反应生成碳酸钠和水,碱性减弱 二氧化碳、水和碳酸钠反应生成碳酸氢钠,碱性继续减弱 取最后段的液体加热至沸腾,将气体通入澄清石灰水 澄清石灰水变浑浊
【解析】
(2)碳酸钠能和氯化钙反应生成碳酸钙沉淀和氯化钠,实验过程如下表所示:
操作 | NaHCO3溶液 | Na2CO3溶液 |
加入稀盐酸 | 产生气泡 | 产生气泡 |
加入稀CaCl2溶液 | 无明显变化 | 产生白色沉淀 |
加热溶液至沸腾,并将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
[进行实验]实验现象是试管内液面上升,结论及化学方程式为:氢氧化钠与二氧化碳反应生成碳酸钠和水,反应方程式为:CO2+2NaOH═Na2CO3+H2O,实验过程如下表所示:
实验操作 | 实验现象 | 结论及化学方程式 |
| 试管内液面上升 | 氢氧化钠与二氧化碳反应生成碳酸钠。反应方程式: |
[实验反思]学习小组讨论,认为产生此实验现象的原因可能有两种:一种是NaOH与CO2发生了反应;另一种是二氧化碳溶于水。
故填:二氧化碳溶于水。
(2)实验检验生成的新物质的方案为:向溶液中加入足量的稀盐酸,产生气泡,说明二氧化碳和氢氧化钠反应生成了碳酸钠,如下表所示:
实验步骤 | 实验现象 | 解释与结论 |
向溶液中加入足量的稀盐酸 | 产生气泡 | NaOH与CO2发生了反应 |
[实验分析](3)AB段变化的原因可能是二氧化碳和氢氧化钠反应生成碳酸钠和水,碱性减弱;
BC段变化的原因可能是二氧化碳、水和碳酸钠反应生成碳酸氢钠,碱性继续减弱。
故填:二氧化碳和氢氧化钠反应生成碳酸钠和水,碱性减弱;二氧化碳、水和碳酸钠反应生成碳酸氢钠,碱性继续减弱。
(4)利用实验验证变化后的产物,实验操作为取最后段的液体加热至沸腾,将气体通入澄清石灰水,实验现象是澄清石灰水变浑浊,实验结论是变化后的产物是碳酸氢钠。
故填:取最后段的液体加热至沸腾,将气体通入澄清石灰水;澄清石灰水变浑浊。

【题目】下列归纳和总结完全正确的一组是( )
A.化学反应基本类型 | B.化学反应中常见的“三” |
①化合反应:4P+5O2 ②分解反应:H2CO3═H2O+CO2↑ ③置换反应:3CO+Fe2O3 | ①煤、石油、天然气,三大化石燃料 ②可燃物、氧气、温度达到着火点,燃烧三条件 ③分子、原子、离子,构成物质的三种粒子 |
C.对鉴别方法的认识 | D.化学与生活 |
①区分氮气和氧气:伸入带火星的木条 ②区分棉纤维和羊毛纤维:点燃后闻气味 ③区分硫酸铵和氯化铵:加熟石灰粉末研磨 | ①用甲醛水溶液浸泡水产品防腐 ②缺乏维生素C易患坏血病 ③自行车支架喷油漆防锈 |
A. AB. BC. CD. D