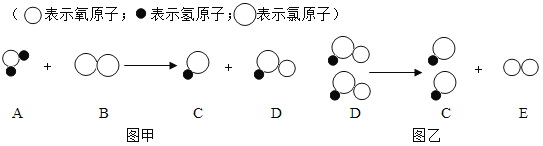
题目内容
【题目】某兴趣小组同学对实验室“过氧化氢分解制氧气”的条件进行了如下探究。
[探究活动1]探究催化剂的种类对过氧化氢分解速率的影响。
设计实验:小组同学设计下列对比实验,实验①:将30g10%过氧化氢溶液与1g二氧化锰均匀混合:实验②将xg 10%过氧化氢溶液与1g氧化铜均匀混合。
实验①中反应的化学方程式是_____;实验②中x的值应为_____。
[探究活动2]探究一些因素对过氧化氢分解速率的影响。
收集证据:小组同学通过实验采集到相关实验数据如下表。
过氧化氢溶液的质量 | 过氧化氢溶液的浓度 | 二氧化锰的质量 | 相同时间内产生氧气体积 | |
Ⅰ | 50. 0g | 1% | 0.1g | 9mL |
Ⅱ | 50. 0g | 2% | 0.1g | 16mL |
Ⅲ | 50. 0g | 4% | 0.1g | 31mL |
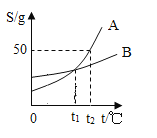
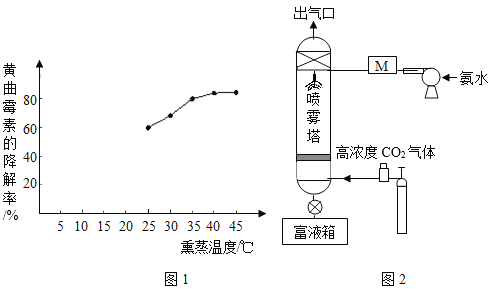
问题与讨论: (1) 本实验的结论是_____。
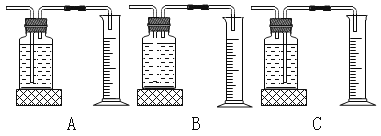
(2)实验时,测量氧气体积的装置应选择下图中_____(填编号)。
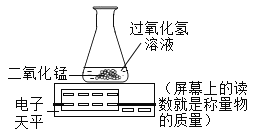
(3)小强同学设计了下图所示装置完成上述实验,通过比较相同时间内_____同样能获取该实验的结论。
【答案】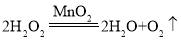 30 在相同的条件下,过氧化氢溶液浓度越高,分解速度越大 C 反应前后屏幕上的读数之差(合理即可)
30 在相同的条件下,过氧化氢溶液浓度越高,分解速度越大 C 反应前后屏幕上的读数之差(合理即可)
【解析】
实验①中过氧化氢在二氧化锰催化作用下反应产生水和氧气的化学方程式是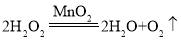 ;实验②中过氧化氢溶液的质量应该与实验①相等,x的值应为30g。
;实验②中过氧化氢溶液的质量应该与实验①相等,x的值应为30g。
问题与讨论: (1)实验Ⅰ、Ⅱ、Ⅲ中唯一的变量就是过氧化氢的浓度, 本实验的结论:在相同的条件下,过氧化氢溶液浓度越高,分解速度越大;
(2)实验时,测量氧气体积的装置应选择:C装置,氧气应该“短管进、长管出”将集气瓶中的水压入量筒中,测量氧气体积;
(3)通过比较相同时间内:反应前后屏幕上的读数之差同样能获取该实验的结论。

【题目】学习质量守恒定律后,某化学兴趣小组的同学利用如图所示的三个实验探究质量守恒定律。
[提出问题]化学反应前后各物质的质量总和是否相等?
[猜想假设]猜想1:不相等;猜想2:相等。
[实验探究]甲、乙、丙三组同学用托盘天平分别称量反应前后物质的质量。
实验方案 | 实验现象 | 结论 | |
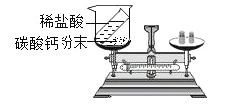
甲组 |
| 产生大量气泡,天平指针向右偏转。 | 不相等。 导致甲组方案反 应前后质量不相等的原因是____________。 |
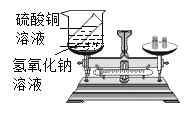
乙组 |
| 产生蓝色沉淀,天平指针_____________。(“向右偏转”、 “向左偏转”或“不发生偏转”) | 相等 |
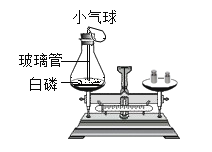
丙组 |
| _____________, 天平指针没有发生偏转。 | 相等 |
[反思评价]在探究化学反应前后各物质的质量总和是否相等时,凡是有气体生成或参加的反应一定要在_____中进行。
[得出结论]甲组同学对装置进行改进后再次探究,亦能得出猜想2正确的结论。经同学们进一步讨论分析发现,反应体系中的反应仪器和未参加反应的物质质量在反应前后保持不变,最终得出结论是:_____________________的各物质的质量总和等于反应后生成的各物质的质量总和。
[微观解释]化学反应前后,原子的_______________________没有改变,原子的数目没有增减,原子的质量没有变化,所以质量守恒。