题目内容
【题目】金属材料在生产、生活中的应用非常广泛.
(1)吃火锅用的锅体是由铜合金制造的,主要是因为铜合金具有很好的________(填序号).
A 导电性 B 导热性 C 延展性
(2)金属锈蚀造成浪费.铁制品锈蚀的过程,实际上是铁与空气中的氧气、___等发生化学反应的过程.
(3)目前世界上已有![]() 以上的废钢铁得到回收利用,其目的是________.
以上的废钢铁得到回收利用,其目的是________.
A 节约金属资源 B 合理开采矿物 C 防止钢铁生锈
(4)实验室有锌片、铁片、铜片、稀硫酸、硫酸锌溶液、硫酸亚铁溶液和硫酸铜溶液![]() 种物质,小红选择合适的物质,设计了以下三种方法对锌、铜、铁的金属活动性顺序进行验证.
种物质,小红选择合适的物质,设计了以下三种方法对锌、铜、铁的金属活动性顺序进行验证.
①方法一所选用的![]() 种物质是________、硫酸锌溶液和硫酸铜溶液.
种物质是________、硫酸锌溶液和硫酸铜溶液.
②方法二所选用的![]() 种物质是锌片、铜片和________.
种物质是锌片、铜片和________.
③方法三所选用![]() 种物质是锌片、铁片、铜片和稀硫酸.
种物质是锌片、铁片、铜片和稀硫酸.
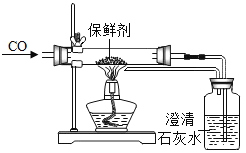
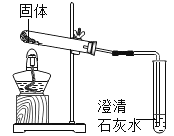
(5)炼铁的原理是利用一氧化碳与氧化铁反应.在实验室里,可用如图所示装置进行实验:实验中玻璃管内的粉末由________色变黑色.
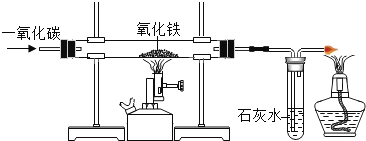
(6)某钢铁厂每天需消耗5000t含Fe2O380%的赤铁矿石,该厂理论上可日产含Fe98%的生铁_____t.(计算结果保留1位小数)
【答案】B 水 A 铁片 硫酸亚铁 红棕色 2857.1
【解析】
(1)火锅的锅体是由铜合金制造的,主要是因为铜合金具有很好的导热性;
(2)铁制品锈蚀的条件:铁与空气中的氧气、水等发生的化学反应;
(3)回收利用金属是为了节约金属资源.
(4))①可以选用的另外一种药品是铁片,铁不与硫酸锌溶液反应,说明锌在铁的前面,铁能与硫酸铜溶液反应,说明铁在铜的前面;
②可以选用的另外一种药品是硫酸亚铁溶液,锌能与硫酸亚铁反应,说明锌在铁的前面,铜不与硫酸亚铁反应,说明铁在铜的前面;
(5)红棕色的氧化铁粉末被还原为黑色的铁粉,一氧化碳与氧化铁反应生成铁和二氧化碳.
(6)解:设理论上可炼出含铁98%的生铁质量为x.
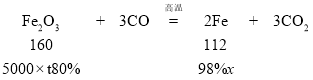
![]()
x≈2857.1t
答:该钢铁厂理论上可日产含Fe98%的生铁质量是2857.1t