题目内容
【题目】黄铁矿(主要成分为FeS2,杂质不含硫元素)是我国大多数硫酸厂制取硫酸的主要原料。化学课外活动小组为测定某黄铁矿中FeS2含量进行了如下的实验探究(假设每步反应均完全)。
【查阅资料】 ①4FeS2+11O2 ![]() 2Fe2O3+8SO2 ②Na2SO3+H2O2=Na2SO4+H2O
2Fe2O3+8SO2 ②Na2SO3+H2O2=Na2SO4+H2O
【实验探究】
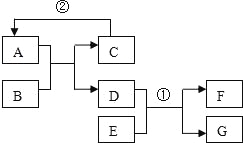
Ⅰ.称取2.40 g黄铁矿样品放入下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。

Ⅱ.反应结束后,将乙瓶中的溶液进行如下处理:

【问题讨论】
(1)Ⅰ装置中甲瓶内盛放的试剂是氢氧化钠溶液,其作用是 。
(2)Ⅰ装置中乙瓶内发生反应的化学反应方程式是 。
【含量测定】
(3)计算该黄铁矿中FeS2的质量分数。(请写出计算过程)
【交流反思】
(4)如果缺少甲装置,则最终测得FeS2的质量分数将会 (填“偏大”“偏小”或“不变”)。
(5)Ⅱ中检验滤渣是否洗涤干净的方法是,取最后一次洗涤液,加入 ,说明已洗涤干净。
【拓展应用】
工业上以黄铁矿为原料生产硫酸的工艺流程图如下所示:

(6)接触室中发生反应的化学方程式为 。化学实验室常需要用到较稀的硫酸,把浓硫酸稀释的操作是 ,硫酸是一种重要的化工产品,用途十分广泛,请写出稀硫酸的一种用途 。
(7)依据生产硫酸的工艺流程图,下列说法正确的是 (填字母)。
A.为使黄铁矿充分燃烧,需将其粉碎
B.催化剂能够提高SO2的反应速率和产量
C.沸腾炉排出的矿渣可供炼铁
D.吸收塔中为了提高吸收效率,采用喷淋的方式
【答案】(1)吸收空气中的二氧化碳
(2)2NaOH + CO2 ==== Na2CO3 + H2O
(3)硫元素的质量:4.66g×32/233=0.64g
FeS2的质量:0.64g/64/120=1.2g
1.2g/2.4g×100%=50%
(4)偏大
(5)滴加硫酸钠溶液,若无白色沉淀,则已洗净。(合理即可)
(6)2SO2+O2=2SO3 酸入水,边加边搅拌 除去金属表面的锈
(7)ACD
【解析】
试题分析:【问题讨论】(1)Ⅰ装置中甲瓶内盛放的试剂是氢氧化钠溶液,其作用是)吸收空气中的二氧化碳;(2)Ⅰ装置中乙瓶内发生反应的化学反应方程式是2NaOH + CO2 ==== Na2CO3 + H2O;(3)硫元素的质量:4.66g×32/233=0.64g ;FeS2的质量:0.64g/64/120=1.2g ;1.2g/2.4g×100%=50%;(4)如果缺少甲装置,空气的二氧化碳会被乙装置吸收,使测量结果偏大,则最终测得FeS2的质量分数将会偏大;(5)Ⅱ中检验滤渣是否洗涤干净,就是判断沉淀表面是否含有氯化钡溶液,故方法是,取最后一次洗涤液,加入滴加硫酸钠溶液,若无白色沉淀,则已洗净。(6)接触室中发生反应的化学方程式为2SO2+O2=2SO3化学实验室常需要用到较稀的硫酸,把浓硫酸稀释的操作是酸入水,边加边搅拌;稀硫酸的一种用途为除去金属表面的锈;(7)依据生产硫酸的工艺流程图,下列说法正确的是A.为使黄铁矿充分燃烧,需将其粉碎C.沸腾炉排出的矿渣可供炼铁D.吸收塔中为了提高吸收效率,采用喷淋的方式;

 阅读快车系列答案
阅读快车系列答案【题目】某班化学实验课进行酸碱盐的性质实验。
〖实验一〗自制酸碱指示剂
(1)取少量紫包菜和白菜叶剪碎后分别在研钵中捣烂,加入酒精溶液浸泡;用纱布将浸泡出的汁液滤出,观察到紫包菜汁液为紫色,白菜汁液为无色。分别装好待用。
(2)取四支试管分别用NaOH溶液和稀盐酸进行实验,观察到现象如图。

记录如下:
NaOH溶液 | 稀盐酸 | |
紫包菜汁液 | ①绿色 | ②红色 |
白菜汁液 | ③无色 | ④淡黄色 |
你认为两种汁液中,更适合做酸碱指示剂的是 。
(3)再用苹果汁进行相同实验,紫包菜汁液变红色,白菜汁液变淡黄色。则苹果汁溶液显 性。
〖实验二〗探究碱和盐的性质
第一组学生进行CuSO4、NaOH溶液的反应,观察到的现象是 ;该反应的化学方程式为 。
第二组学生进行BaCl2、Na2CO3溶液的反应,反应的化学方程式为 。
〖实验三〗废液再探究
〖实验二〗结束后,两组同学将全部的废液集中倒进一个废液缸中。兴趣小组同学对废液进行过滤,得到无色滤液。
【提出问题】
滤液中含有什么溶质?
【做出猜想】
滤液中一定含有 ,还可能含有BaCl2、NaOH、Na2CO3、Na2SO4中的一种或几种。
【实验探究】
(1)取少量滤液加入试管中,滴加紫包菜汁液,溶液显绿色。
(2)继续加入足量的稀硫酸,溶液变成红色,无气泡和沉淀产生,则滤液中一定没有 。根据(1)(2)判断滤液中一定含有 。
(3)为最终确定该滤液的组成,还需补充的实验是: ,观察到白色沉淀。
【实验结论】 该无色滤液的组成为 。
【题目】氢氧化钠和氢氧化钙是两种常见的碱.小林将两种碱的溶液分别装入试管A、B 中,进行如下实验.

(1)实验l 中,两支试管的溶液都变成 色.
(2)实验2中,若B盛装的是氢氧化钠溶液,发生反应的化学方程式是 .
(3)实验3中,小林向两支试管中吹气,A中有白色沉淀生成,发生反应的化学方程式是 .B中无现象,为探究吹气后B中溶质的成分,小林进行如下探究:
【提出猜想】猜想1:溶质只有氢氧化钠
猜想2:溶质只有碳酸钠
猜想3:溶质有氢氧化钠和碳酸钠
【实验和结论】
实验 | 实验现象 | 结论 |
取B中少量溶液,加入澄清石灰水至不再产生沉淀为止,过滤后取上层清液,向其中加几滴酚酞溶液. | 产生白色沉淀 溶液呈现红色 | 猜想3成立 |
【反思与评价】老师评价小林得出的结论不正确,是因为 .
如果要验证猜想3成立,你的改进意见是 .